题目内容
14.含有共价键的分子晶体是( )| A. | NaOH | B. | SiO2 | C. | Cl2 | D. | NH4Cl |
分析 分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体.常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等.
解答 解:A、NaOH晶体是由钠离子和氢氧根离子组成的离子晶体,故A错误;
B、二氧化硅是由Si和O以共价键结合在一起的原子晶体,故B错误;
C、氯气是仅含共价键构成的分子晶体,故C正确;
D、氯化铵中含有离子键晶体,故D错误;
故选C.
点评 本题考查常见物质晶体类型判断等,难度不大,掌握常见物质晶体类型及常见分子晶体.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
4.下列关于原电池的叙述中正确的是( )
| A. | 正极和负极必须是两种不同的金属 | |
| B. | 电子流入的一极为正极 | |
| C. | 原电池工作时,正极和负极上发生的都是氧化还原反应 | |
| D. | 锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢气生成 |
5.如图是元素周期表中短周期的一部分,若A原子最外层的电子数比次外层少3,则下列说法正确的是( )
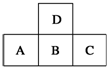

| A. | 原子半径的大小顺序是C>B>A>D | |
| B. | B、D之间只能形成一种化合物 | |
| C. | 只有A的单质存在同素异形体 | |
| D. | A、B、C的最高价氧化物对应水化物的酸性强弱的关系是C>B>A |
2.下列物质熔化时不需要破坏化学键的是( )
| A. | NaOH | B. | SiO2 | C. | Mg | D. | CH4 |
9.下列四组物质的分子式都相同,按物质的分类方法属于同一类物质的是( )
| A. | 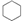 和CH2CH-CH2CH2CH2CH3 和CH2CH-CH2CH2CH2CH3 | B. | 正戊烷和新戊烷 | ||
| C. | CH3-O-CH3和CH3CH2OH | D. | 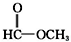 和 和 |
19.下列关于化学能转化为电能的四种装置的说法正确的是( )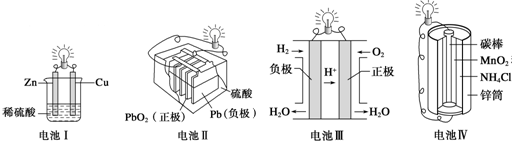

| A. | 电池Ⅰ中锌是负极 | |
| B. | 电池Ⅱ是一次电池 | |
| C. | 电池Ⅲ工作时氢气发生还原反应 | |
| D. | 电池Ⅳ工作时电子由锌通过导线流向碳棒 |
6.元素X原子的最外层有4个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物的化学式可能是( )
| A. | XY2 | B. | X2Y3 | C. | X3Y2 | D. | X2Y |
3.下列说法不正确的是( )
| A. | 分子间作用力是分子间相互作用力的总称 | |
| B. | 范德华力与氢键可同时存在于分子之间 | |
| C. | 分子间氢键的形成除使物质的熔沸点升高外,对物质的溶解度、硬度等也有影响 | |
| D. | 氢键是一种特殊的化学键,它广泛地存在于自然界中 |
4.下列物质属于同系物的是( )
| A. | 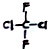 和 和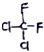 | B. | CH3CH2Cl和CH2ClCH2Cl | ||
| C. | C2H6和C5H12 | D. | CH3CH2OH和CH3Cl |