题目内容
试解释:在酸性介质中,Co3+能氧化Cl-;但[Co(NH3)6]3+却不能.
考点:氧化还原反应
专题:
分析:Co3+含有空轨道、氨气分子中N原子含有孤电子对,Co3+和氨气分子能形成配合物,配离子没有氧化性,Co3+浓度越大其氧化性越强,据此分析解答.
解答:
解:Co3+含有空轨道、氨气分子中N原子含有孤电子对,Co3+和氨气分子能形成配合物,配离子没有氧化性,Co3+浓度越大其氧化性越强,形成配合物[Co(NH3)6]3+后,大大降低了Co3+的浓度,所以[Co(NH3)6]3+不能氧化Cl-,
答:形成配合物[Co(NH3)6]3+后,大大降低了Co3+的浓度,故[Co(NH3)6]3+不能氧化Cl-.
答:形成配合物[Co(NH3)6]3+后,大大降低了Co3+的浓度,故[Co(NH3)6]3+不能氧化Cl-.
点评:本题考查氧化还原反应、配合物的形成等知识点,明确配合物形成条件及物质性质即可解答,知道常见配合物,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
同周期的X、Y、Z三元素,它们最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
| A、含氧酸的酸性H3ZO4>H2YO4>HXO4 |
| B、非金属性X>Y>Z |
| C、元素的负化合价的绝对值按X、Y、Z变小 |
| D、气态氢化物的稳定性按X、Y、Z的顺序增强 |
设NA为阿佛加德罗常数,下列叙述正确的( )
| A、标准状况下,NA个SO3分子所占的体积约为22.4 L |
| B、5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C、铁粉与一定量的浓硫酸反应,若产生11.2 L SO2和1 g H2,铁粉失去的电子数为2NA |
| D、50 mL 12 mol?L-1 浓盐酸与足量二氧化锰反应,转移电子数为0.3 NA |
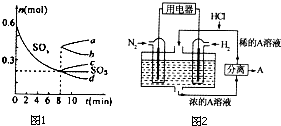 运用化学反应原理研究碳、氮、硫等单质及其化合物的反应有重要意义;
运用化学反应原理研究碳、氮、硫等单质及其化合物的反应有重要意义;
