题目内容
5.在下列各组物质中,只有还原性的是( )| A. | Na、Cl-、S2- | B. | Cl-、CO、Na+ | C. | Fe3+、SO42-、NO3- | D. | Fe2+、O2、H2S |
分析 化合价处于最高价态的元素只能得电子体现氧化性,化合价处于最低价态的元素只能失电子体现还原性,处于中间价态的元素既能得电子又能失电子,所以体现氧化性和还原性,据此分析解答.
解答 解:A、这几种微粒化合价都处于最低价态,所以只能作还原剂体现还原性,故A正确;
B、钠离子中Na元素化合价处于最高价态,则只有氧化性,故B错误;
C、硫酸根离子中S元素、硝酸根离子中N元素化合价都处于最高价态,则只能得电子体现氧化性,故C错误;
D、亚铁离子中Fe元素化合价处于中间价态,既有氧化性又有还原性,氧气中O元素化合价处于最高价态,所以只有氧化性,硫化氢中S元素处于最低价态、H元素处于最高价态,所以硫化氢具有氧化性和还原性,故D错误;
故选A.
点评 本题考查氧化性、还原性判断,明确元素化合价与元素性质的关系即可解答,熟练常见元素化合价,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列共价键中,属于非极性键的是( )
| A. | C-H | B. | C-Cl | C. | C═O | D. | N≡N |
13.下列离子方程式正确的是( )
| A. | 铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 硫酸钠溶液和氯化钡溶液反应:Ba2++SO42-=BaSO4↓ |
10.0.1mol铜与40mL 10mol•L-1 HNO3充分反应后,溶液中含a mol H+,由此可知( )
| A. | 生成的气体在标准状况下的体积为4.48 L | |
| B. | 硝酸只起到强氧化性作用 | |
| C. | 被还原的硝酸的物质的量为(0.2-a) mol | |
| D. | 反应后溶液中所含NO3-的物质的量为0.2 mol |
17.乙醇分子中各种化学键如图所示.下列有关反应断键位置说明错误的是( )


| A. | 乙醇和浓硫酸,共热到170℃时断键②⑤ | |
| B. | 乙醇和浓硫酸,共热到140℃时断键①④ | |
| C. | 乙醇和金属钠的反应断键① | |
| D. | 乙醇在Cu催化下与O2反应时断键①③ |
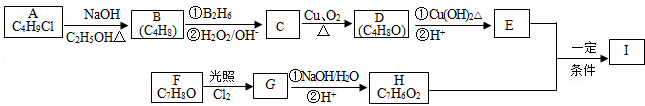
 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
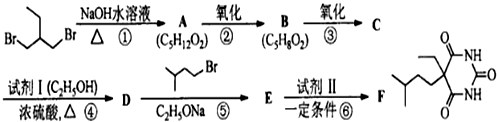
.
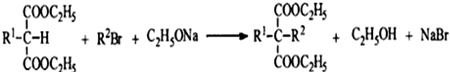 (R1,R2代表烷基)
(R1,R2代表烷基)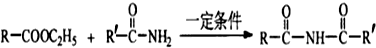 (其他产物略)
(其他产物略) .
.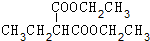 +(CH3)2CHCH2CH2Br+CH3CH2ONa→
+(CH3)2CHCH2CH2Br+CH3CH2ONa→ +CH3CH2OH+NaBr.
+CH3CH2OH+NaBr. .
. .
.