��Ŀ����
14����1����֪����CO��g��+H2O��g��?H2��g��+CO2��g����H=-41kJ•mol-1��C��s��+2H2��g��?CH4��g����H=-73kJ•mol-1
��2CO��g��?C��s��+CO2��g����H=-171kJ•mol-1
��CO2��g��+4H2��g���TCH4��g��+2H2O��g����H=-162kJ•mol-1��
��2������������ͬʱ��CO��H2�����ʵ�����1��3���з�Ӧ��CO��g��+3H2��g��?CH4��g��+H2O��g��
H2��ƽ��ת�����ڲ�ͬѹǿ�£����¶ȵı仯��ͼ1��ʾ��

��ʵ�������в���ͼ��M�������N���Ӧ�ķ�Ӧ���������û�ѧ��Ӧ���ʺ�ƽ��֪ʶ��ͬʱ��������ʵ�ʣ�˵��ѡ��÷�Ӧ������������N��������ȣ�ѡ��M������ʱ����ȻH2ת���ʵ�Щ�����¶Ƚϸߣ���Ӧ���ʽϿ죬ѹǿΪ��ѹ���豸Ҫ�ߣ��ۺϳɱ��ͣ�
��M���ƽ�ⳣ��Kp=$\frac{\frac{0.9}{2.2}��1.01��1{0}^{5}��\frac{0.9}{2.2}��1.01��1{0}^{5}}{\frac{0.1}{2.2}��1.01��1{0}^{5}����\frac{0.3}{2.2}��1.01��1{0}^{5}��^{3}}$����ֻ����ʽ��Kp�ı���ʽ�ǽ�ƽ���ѹ����ƽ��Ũ�ȣ�ij���ʵ�ƽ���ѹ=��ѹ�������ʵ����ʵ���������
��3��ͼ2��ʾ��һ�������µ�1L���ܱ������У�X��Y��C��������������Ӧ��������������ʵ�����ʱ��ı仯������±���3molX��1molY��һ���¶Ⱥ�һ��ѹǿ�·�Ӧ���ﵽƽ��ʱC�����������C%����
| ѹǿ/Mpa C% �¶�/�� | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
�ڱ���a��ȡֵ��Χ��25.1��a��64.2��
�۸�����ͼ���ϱ�������25min��40min��ͼ�����߷����仯��ԭ���������С�������������ѹǿ��
���� ��1�������Ȼ�ѧ����ʽ��˹���ɼ����+��-�١�2 �õ��õ������Ȼ�ѧ����ʽ��
��2���������Ȼ�ѧ����ʽ��ϸ�˹���ɼ���õ��Ȼ�ѧ����ʽ��CO��g��+3H2��g��?CH4��g��+H2O��g������Ӧ����̬�����С��Ӧ�����Ӱ�컯ѧ��Ӧ���ʡ��������ԡ�ѹǿ���豸������Ч�������
��Kp�ı���ʽ�ǽ�ƽ���ѹ����ƽ��Ũ�ȣ�ij���ʵ�ƽ���ѹ=��ѹ�������ʵ����ʵ���������
��3����ͼ�������֪XYΪ��Ӧ�CΪ�����X���ʵ�������3mol-9��0.25mol=0.75mol��Y�������ʵ���=0.25mol��C�������ʵ���Ϊ0.5mol�����ʵ���֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ��ݴ�д����ѧ����ʽ��
��Y+3X?2C����Ӧ�����������С�ķ�Ӧ������һ��������ͼ���������жϣ��¶�һ��C%��ѹǿ�仯��ѹǿһ�����¶ȱ仯C%�仯�õ�a��ȡֵ��
��25min��40min��ͼ�����߷����仯��XY������������C��������������������ѹǿ��������ƽ��������У�XY���ʵ�����С��C���ʵ������ӣ�
��� �⣺��1����CO��g��+H2O��g��?H2��g��+CO2��g����H=-41kJ•mol-1
��C��s��+2H2��g��?CH4��g����H=-73kJ•mol-1
��2CO��g��?C��s��+CO2��g����H=-171kJ•mol-1
��˹���ɼ����+��-�١�2 �õ�CO2��g��+4H2��g���TCH4��g��+2H2O��g����H=-162 kJ•mol-1��
�ʴ�Ϊ��-162 kJ•mol-1��
��2�������ݸ�˹���ɼ��㣬
��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41kJ•mol-1
��C��s��+2H2��g��?CH4��g����H=-73kJ•mol-1
��2CO��g��?C��s��+CO2��g����H=-171kJ•mol-1
��+��-�ٵõ�CO��g��+3H2��g��?CH4��g��+H2O��g������H=-203KJ/mol
��Ӧ����̬�����С�ķ��ȷ�Ӧ�����¸�ѹ�ٽ�ƽ��������У�ͼ�������֪����N��������ȣ�ѡ��M������ʱ����ȻH2ת���ʵ�Щ�����¶Ƚϸߣ���Ӧ���ʽϿ죬ѹǿΪ��ѹ���豸Ҫ�ߣ��ۺϳɱ��ͣ�
�ʴ�Ϊ����N��������ȣ�ѡ��M������ʱ����ȻH2ת���ʵ�Щ�����¶Ƚϸߣ���Ӧ���ʽϿ죬ѹǿΪ��ѹ���豸Ҫ�ߣ��ۺϳɱ��ͣ�
��M������ת����Ϊ90%��CO��H2�����ʵ�����1��3����Ϊ1mol��3mol����ϻ�ѧ��Ӧ���м���õ�ƽ�����ʵ������������ʵ�ƽ���ѹ=��ѹ�������ʵ����ʵ����������õ�ƽ�ⳣ����ѹǿΪ1.01��105��
CO��g��+3H2��g��?CH4��g��+H2O��g��
��ʼ����mol�� 1 3 0 0
�仯����mol�� 0.9 2.7 0.9 0.9
ƽ������mol�� 0.1 0.3 0.9 0.9
�����ʵ���=2.2mol��
M���ƽ�ⳣ��Kp=$\frac{\frac{0.9}{2.2}��1.01��1{0}^{5}��\frac{0.9}{2.2}��1.01��1{0}^{5}}{\frac{0.1}{2.2}��1.01��1{0}^{5}����\frac{0.3}{2.2}��1.01��1{0}^{5}��^{3}}$
�ʴ�Ϊ��$\frac{\frac{0.9}{2.2}��1.01��1{0}^{5}��\frac{0.9}{2.2}��1.01��1{0}^{5}}{\frac{0.1}{2.2}��1.01��1{0}^{5}����\frac{0.3}{2.2}��1.01��1{0}^{5}��^{3}}$��
��3����ͼ�������֪XYΪ��Ӧ�CΪ�����X���ʵ�������3mol-9��0.25mol=0.75mol��Y�������ʵ���=0.25mol��C�������ʵ���Ϊ0.5mol�����ʵ���֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ��ݴ�д����ѧ����ʽ��Y+3X?2C��
�ʴ�Ϊ��Y+3X?2C��
��Y+3X?2C����Ӧ�����������С�ķ�Ӧ��ѹǿһ�����¶�����C�����������С��˵������ӦΪ���ȷ�Ӧ��10Mpa���¶�����ƽ���������C���������С��a��25.1��ͼ�����¶�һ��ѹǿ����ƽ��������У�a��64.2����aȡֵ25.1��a��64.2��
�ʴ�Ϊ��25.1��a��64.2��
��25min��40min��ͼ�����߷����仯��XY������������C��������������������ѹǿ��������ƽ��������У�XY���ʵ�����С��C���ʵ������ӣ��ı����������С�������������ѹǿ��
�ʴ�Ϊ����С�������������ѹǿ��
���� ���⿼���˻�ѧ��Ӧ�Ȼ�ѧ����ʽ���ʱ�ļ��������ƽ��Ӱ�����ء�ƽ�ⳣ�����㡢ͼ��仯�����ݱ仯���жϣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

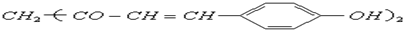 �������Ƴɵ���ֽ���Լ�����Һ������ԣ��ܹ���1mol�û�������Ӧ��Br2ˮ��Һ��H2����������ֱ��ǣ�������
�������Ƴɵ���ֽ���Լ�����Һ������ԣ��ܹ���1mol�û�������Ӧ��Br2ˮ��Һ��H2����������ֱ��ǣ�������| A�� | 3mol 3mol | B�� | 3mol 5mol | C�� | 6 mol 10 mol | D�� | 6 mol 8 mol |
| A�� | 1-�嶡�� | B�� | 2-��-3-������ | ||
| C�� | 2��2-����-1-�ȶ��� | D�� | һ�ȼ��� |
| A�� | �����ӻ������ֻ�������Ӽ���û�й��ۼ� | |
| B�� | �Ǽ��Լ�ֻ������˫ԭ�ӵĵ��ʷ����� | |
| C�� | �κ������ﶼ���л�ѧ�� | |
| D�� | �ڹ��ۻ���������ڣ�һ�����������Ӽ� |
| Y | V | |||
| X | W |
| A�� | ԭ�Ӱ뾶��X��W��V��Y | |
| B�� | Y�����������ĵ���ʽΪ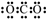 | |
| C�� | X���������������V��W����������Ӧ��ˮ���ﷴӦ | |
| D�� | �ס��һ��ʱ�����ɵ�����Ϊ���ӻ�����Ⱥ������Ӽ��ֺ��зǼ��Լ� |
| ѡ�� | ʵ����� | ���� | ���� |
| A | ��ij����ͨ��FeCl2��Һ�� | ��Һ��dz��ɫ��Ϊ��ɫ | ��������һ������Cl2 |
| B | ��ij����ͨ��Ʒ����Һ�� | Ʒ����Һ��ɫ | ��������һ������SO2 |
| C | ��ij����ͨ�����ȵ�CuO��ĩ | ��ĩ�ɺڱ�� | ��������һ������H2 |
| D | ��ij������ʪ��ĺ�ɫʯ����ֽ�Ӵ� | ��ֽ����ɫ | ��������һ������NH3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
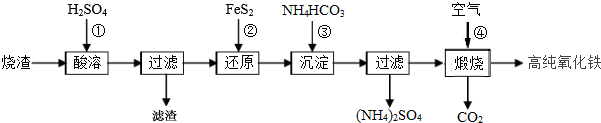

 ������ṹ���ýṹ�Ķ��ȴ�����3�֣�
������ṹ���ýṹ�Ķ��ȴ�����3�֣� ���ýṹ��ʽ���ܽ�����������A��ʵ�����ţ���
���ýṹ��ʽ���ܽ�����������A��ʵ�����ţ���