题目内容
下列离子方程式正确的是( )
| A、把少量铜屑放入稀硝酸中:Cu+4H++2 NO3-═Cu2++2NO2↑+2H2O |
| B、将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| C、在NaOH浓溶液中滴入几滴NH4Cl溶液:NH4++OH-═NH3↑+H2O |
| D、将少量SO2通入漂白粉溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
考点:离子方程式的书写
专题:离子反应专题
分析:A.铜和稀硝酸反应生成NO;
B.铜和稀硫酸不反应;
C.二者反应生成氨气和水;
D.二者发生氧化还原生成硫酸钙和盐酸.
B.铜和稀硫酸不反应;
C.二者反应生成氨气和水;
D.二者发生氧化还原生成硫酸钙和盐酸.
解答:
解:A.铜和稀硝酸反应生成NO,离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故A错误;
B.铜和稀硫酸不反应,所以没有离子方程式,故B错误;
C.二者反应生成氨气和水,离子方程式为NH4++OH-═NH3↑+H2O,故C正确;
D.二者发生氧化还原生成硫酸钙和盐酸,离子方程式为SO2 +ClO-+Ca2++H2O=CaSO4↓+Cl-+2H+,故D错误;
故选C.
B.铜和稀硫酸不反应,所以没有离子方程式,故B错误;
C.二者反应生成氨气和水,离子方程式为NH4++OH-═NH3↑+H2O,故C正确;
D.二者发生氧化还原生成硫酸钙和盐酸,离子方程式为SO2 +ClO-+Ca2++H2O=CaSO4↓+Cl-+2H+,故D错误;
故选C.
点评:本题考查了离子方程式正误判断,明确物质的性质及物质间的反应、离子反应书写规则即可解答,注意铜和硝酸的产物与硝酸浓度有关,易错选项是D,注意次氯酸根离子能氧化二氧化硫,C中如果氢氧化钠是稀溶液就生成一水合氨,这些都是易错点.

练习册系列答案
相关题目
下列各组微粒具有相同的质子数和电子数的是( )
| A、OH-、H2O |
| B、NH4+、NH2- |
| C、H3O+、CH4 |
| D、HCl、F2 |
下列说法不正确的是( )
| A、“地沟油”经加工处理后,可用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
| B、蔗糖、淀粉、油脂及其水解产物中既有电解质也有非电解质 |
| C、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D、离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 |
下列化学用语表达正确的是( )
| A、一氯乙烷的结构式CH3Cl |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的电子式 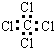 |
D、C2H4分子比例模型: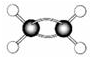 |
常温下,下列溶液中可能大量共存的离子组是( )
| A、加入金属镁能产生H2的溶液中:Na+、Fe2+、SO42-、NO3- |
| B、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
| C、水电离产生的c(OH-)=1×10-10mol/L的溶液中:Al3+、SO42-、NO3-、Cl- |
| D、能使Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3- |
长周期元素周期表共有18个竖行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法正确的是( )
| A、第13列元素中没有非金属 |
| B、第15列元素的原子最外层的排布是ns2np3 |
| C、最外层电子数为ns2的元素在第2列 |
| D、10、11列为ds区的元素 |