题目内容
长周期元素周期表共有18个竖行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法正确的是( )
| A、第13列元素中没有非金属 |
| B、第15列元素的原子最外层的排布是ns2np3 |
| C、最外层电子数为ns2的元素在第2列 |
| D、10、11列为ds区的元素 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A.第13列元素为ⅢA元素;
B.第15列为第ⅤA族,属于p区,最外层电子数等于族序数;
C.最外层电子数为ns2的元素可能为He,也可能为ⅡA族元素;
D.第10列为第ⅤⅢ族元素,第11列为第ⅠB族元素.
B.第15列为第ⅤA族,属于p区,最外层电子数等于族序数;
C.最外层电子数为ns2的元素可能为He,也可能为ⅡA族元素;
D.第10列为第ⅤⅢ族元素,第11列为第ⅠB族元素.
解答:
解:A.第13列元素为ⅢA元素,B为非金属元素,其它为金属元素,故A错误;
B.第15列为第ⅤA族,属于p区,最外层电子数等于族序数,最外层电子排布为ns2 np3,故B正确;
C.最外层电子数为ns2的元素可能为He,也可能为ⅡA族元素,第2列是第ⅡA族,最外层电子排布为ns2,He处于零族,He原子的核外电子排布为1s2,一些过渡元素的最外层电子排布为ns2,故C错误;
D.第10列为第ⅤⅢ族元素,为d区元素;第11列为第ⅠB族元素,为ds区元素,故D错误;
故选B.
B.第15列为第ⅤA族,属于p区,最外层电子数等于族序数,最外层电子排布为ns2 np3,故B正确;
C.最外层电子数为ns2的元素可能为He,也可能为ⅡA族元素,第2列是第ⅡA族,最外层电子排布为ns2,He处于零族,He原子的核外电子排布为1s2,一些过渡元素的最外层电子排布为ns2,故C错误;
D.第10列为第ⅤⅢ族元素,为d区元素;第11列为第ⅠB族元素,为ds区元素,故D错误;
故选B.
点评:本题考查元素周期表的结构及应用,为高频考点,注意整体把握元素周期表及列与族的关系,选项D为解答的难点,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列离子方程式正确的是( )
| A、把少量铜屑放入稀硝酸中:Cu+4H++2 NO3-═Cu2++2NO2↑+2H2O |
| B、将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| C、在NaOH浓溶液中滴入几滴NH4Cl溶液:NH4++OH-═NH3↑+H2O |
| D、将少量SO2通入漂白粉溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
下列叙述正确的是( )


| A、Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应 |
| B、图一所示当有0.1mol电子转移时,有0.1mol Cu2O生成 |
| C、图二装置中发生:Cu+2Fe3+═Cu2++2Fe2+,X极是负极,Y极材料可以是铜 |
| D、如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中 |
处于固体状态的下列物质,其晶体类型正确的一组是 ( )
| 离子晶体 | 分子晶体 | 原子晶体 | |
| A | KOH | SO3 | Ar |
| B | H2SO4 | 硫磺 | 石墨 |
| C | CH3COONH4 | H2O | 水晶 |
| D | Ba(OH)2 | 玻璃 | 金刚石 |
| A、A | B、B | C、C | D、D |
下列说法不正确的是( )
| A、2011年诺贝尔化学奖授予以色列科学家达尼埃尔?谢赫特曼,以表彰他发现了准晶体.化学式为Al63Cu24Fe13的准晶体可与稀硝酸发生反应. |
| B、分光光度计可用于分析溶液颜色与反应物(或生成物)浓度的关系,从而确定化学反应速率 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 |
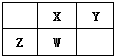 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )| A、W位于第三周期IV族 |
| B、Y的气态氢化物的水溶液中只存在两个平衡状态 |
C、X的最高价氧化物的电子式是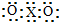 |
| D、常温下,将Z单质投入到Y的最高价氧化物对应的水化物的浓溶液中,无明显现象 |
某元素X的气态氢化物的化学式为XH4,则X的最高价氧化物的水化物的化学式为( )
| A、H3XO4 |
| B、H2XO4 |
| C、H2XO3 |
| D、HXO3 |
 X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol?L-1D溶液的pH为13(25℃).它们满足如图转化关系,则下列说法正确的是( )
X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol?L-1D溶液的pH为13(25℃).它们满足如图转化关系,则下列说法正确的是( )| A、原子半径W>Z>Y>X |
| B、化合物F中含有共价键和离子键 |
| C、在B和C的反应中,氧化剂是B,还原剂是C |
| D、Z元素的最高正价为+6 |
下列物质互为同分异构体的是( )
| A、葡萄糖和果糖 |
| B、淀粉和纤维素 |
| C、氧气和臭氧 |
| D、乙烷和丙烷 |