题目内容
1. 工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示:
工业上和净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为:CO(g)+H2O(g)?H2(g)+CO2(g).一定条件下,将4molCO与2molH2O(g)充入体积为2L的密闭容器中,体系中各物质的深度随时间变化如图所示:(1)在0~4min时段,反应速率v(H2O)为0.2mol•min-1,该条件下反应的平衡常数K为2.7(保留两位有效数字).
(2)该反应到4min时,CO的转化率为40%.
(3)若6min时改变的外部条件为升温,则该反应的△H<0(填“>”、“=”或“<”),此时反应的平衡常数减小(填“增大”、“减小”或“不变”).
(4)判断该反应达到化学平衡状态的依据是b.
a.混合气体的密度不变
b.混合气体中c(CO)不变
c.v(H2O)正=v(H2)正
d.断裂2molH-O键的同时生成1molH-H键
(5)若保持与4min时相同的温度,向一容积可变的密闭容器中同时充入0.5molCO、1.5molH2O(g)、0.5molCO2和amolH2,则当a=2.5时,上述反应向正反应(填“正反应”或“逆反应”)方向进行.若要使上述反应开始时向逆反应进行,则a的取值范围为a>4.05.
分析 (1)图象分析可知4min反应达到平衡状态,物质浓度为c(CO)=1.2mol/L,c(H2)=0.8mol/L,c(H2O)=0.2mol/L,结合化学平衡三段式列式计算平衡浓度,反应速率V=$\frac{△c}{△t}$,平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;
(2)依据(1)的计算结果得到转化率=$\frac{消耗量}{起始量}$×100%;
(3)若6min时改变的外部条件为升温,图象可知氢气浓度减小,一氧化碳和水的浓度增大,说明平衡逆向进行,依据化学平衡移动原理分析;
(4)平衡标志是正逆反应速率相同,各组分含量保持不变,反应过程中“变量不变”分析选项;
(5)计算浓度商和平衡常数比较大小分析判断反应进行的方向,浓度商大于平衡常数正向进行,小于平衡常数逆向进行;
解答 解:(1)图象分析可知4min反应达到平衡状态,物质浓度为c(CO)=1.2mol/L,c(H2)=0.8mol/L,c(H2O)=0.2mol/L,结合化学平衡三段式列式计算平衡浓度,
CO(g)+H2O(g)?H2(g)+CO2(g)
起始量(mol/L) 2 1 0 0
变化量(mol/L) 0.8 0.8 0.8 0.8
平衡量(mol/L) 1.2 0.2 0.8 0.8
在0~4min时段,反应速率v(H2O)=$\frac{△c}{△t}$=$\frac{0.8mol/L}{4min}$=0.2mol/(L•min),
平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$=$\frac{0.8×0.8}{1.2×0.2}$=2.7;
故答案为:0.2mol/(L•min);2.7;
(2)该反应到4min时,CO的转化率=$\frac{0.8mol/L}{2mol/L}$×100%=40%;
故答案为:40%;
(3)若6min时改变的外部条件为升温,图象可知氢气浓度减小,一氧化碳和水的浓度增大,说明平衡逆向进行,逆向为吸热反应,正反应为放热反应,则该反应的△H<0,此时平衡逆向进行,平衡常数减小;
故答案为:<,减小;
(4)上述分析可知,反应CO(g)+H2O(g)?H2(g)+CO2(g)是气体体积不变的放热反应
a.反应前后气体质量和体积不变,混合气体的密度始终不变,不能说明反应达到平衡状态,故a错误;
b.混合气体中c(CO)不变是平衡的标志,故b正确;
c.v(H2O)正=v(H2)正,反应速率之比等于化学方程式计量数之比,为正反应速率之比,只能说明反应正向进行,不能证明正逆反应速率相同,故c错误;
d.断裂2molH-O键的同时生成1molH-H键,说明反应正向进行,不能这么说明正逆反应速率相同,故d错误;
故答案为:b;
(5)若保持与4min时相同的温度,向一容积可变的密闭容器中同时充入0.5molCO、1.5molH2O(g)、0.5molCO2和amolH2,则当a=2.5时,Q=$\frac{2.5×0.5}{0.5×1.5}$=1.7<K=2.7,说明反应正向进行;若要使上述反应开始时向逆反应进行,Q=$\frac{a×0.5}{0.5×1.5}$>2.7,则a的取值范围为a>4.05;
故答案为:正反应;a>4.05.
点评 本题考查了化学平衡的分析应用,主要是图象分析,平衡常数、反应速率的概念计算应用,注意一下化学平衡的因素分析判断,掌握基础是解题关键,题目难度中等.

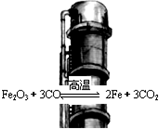
| A. | 升高温度,反应速率减慢 | |
| B. | 当反应达到化学平衡时,υ(正)=υ(逆)=0 | |
| C. | 提高炼铁高炉的高度可减少尾气中CO的浓度 | |
| D. | 某温度下达到平衡时,CO的体积分数基本不变 |
| A. | KAl(SO4)2 | B. | NH4Al(SO4)2 | C. | (NH4)2Fe(SO4)2 | D. | NH4Fe(SO4)2 |
| 阳离子 | NH4+、K+、Al3+、Mg2+ |
| 阴离子 | HCO3-、Cl-、MnO4-、SO42- |
①取10mL该溶液试管中,滴加足量的Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03mol白色沉淀甲.
②取上述反应后滤液,加入AgNO3溶液未见沉淀产生.
③另取10mL该溶液于试管中,滴加NaOH溶液产生白色产生乙,当加入NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,气体丙逸出,将收集的气体丙的体积换算成标准状况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.
下列推断不正确的是( )
| A. | 肯定没有Mg2+、HCO3-、Cl-、MnO4- | |
| B. | 一定含有K+,且c(K+)=2mol/L | |
| C. | 该溶液可能是KAl(SO4)2和NH4Al(SO4)2的混合溶液 | |
| D. | 若仅根据实验③,将该溶液蒸干、灼烧,有可能得到仅含有氧化铝固体物质 |
| A. | 非金属元素的原子最外层电子数都大于或等于4 | |
| B. | 只有非金属能形成含氧酸或含氧酸盐 | |
| C. | Na2O2中阴阳离子的个数比为1:1 | |
| D. | 非金属元素组成的化合物不一定是共价化合物 |
| A. | 增加体系的压强 | B. | 减少C的物质的量浓度 | ||
| C. | 增加A的物质的量 | D. | 升高体系的温度 |
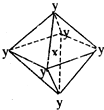 在某晶体中,与某一种微粒x距离最近且等距离的另一种微粒y所围成的空间构型为正八面体型(如图).该晶体可能为( )
在某晶体中,与某一种微粒x距离最近且等距离的另一种微粒y所围成的空间构型为正八面体型(如图).该晶体可能为( )| A. | NaCl | B. | CsCl | C. | CO2 | D. | SiO2 |
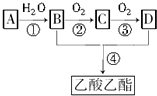 已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;
已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;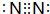 .
.