题目内容
可逆反应2NO2?O2+2NO在密闭容器中反应,达到平衡状态的标志是( )
| A、NO2、NO和O2 三者共存 |
| B、单位时间内生成2mol NO同时消耗2mol NO2 |
| C、v(NO2)正=2v(O2)逆 |
| D、容器中的各物质物质的量浓度之比为2:2:1的状态 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、可逆反应是反应物和生成物共存的体系,未平衡时就是三者共存的体系,故A错误;
B、单位时间内生成2mol NO等效于消耗2mol NO2同时消耗2mol NO2,未平衡时就是一个不变的量,未体现正逆的关系,故B错误;
C、v(NO2)正=2v(O2)正=2v(O2)逆,故C正确;
D、当体系达平衡状态时,容器中的各物质物质的量浓度之比可能为2:2:1的状态,也可能不是2:2:1,与各物质的初始浓度及转化率有关,故D错误;
故选C.
B、单位时间内生成2mol NO等效于消耗2mol NO2同时消耗2mol NO2,未平衡时就是一个不变的量,未体现正逆的关系,故B错误;
C、v(NO2)正=2v(O2)正=2v(O2)逆,故C正确;
D、当体系达平衡状态时,容器中的各物质物质的量浓度之比可能为2:2:1的状态,也可能不是2:2:1,与各物质的初始浓度及转化率有关,故D错误;
故选C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
鉴别二甲醚和乙醇可采用化学方法或物理方法,下列方法不能对二者进行鉴别的是( )
| A、利用金属钠或金属钾法 |
| B、利用红外光谱法 |
| C、利用质谱法 |
| D、利用核磁共振氢谱法 |
化学来源于生活,应用于生活,渗透在生活的各个领域.下列有关物质的性质与应用的说法不相对应的是( )
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、FeCl3溶液能与铜反应,可用于蚀刻印刷电路板 |
| C、碳酸氢钠可与盐酸反应,可用作抗酸药 |
| D、SiO2具有良好的导电性,可用作光导纤维 |
下列措施中,能加快化学反应速率的是( )
| A、将食物储存在冰箱里 |
| B、用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 |
| C、往H2O2溶液中加入少量MnO2 |
| D、用纯锌代替粗锌与1mol/L H2SO4溶液反应 |
已知25℃、101kPa条件下:
4Al(s)+3O2(g)═2Al2O3(s)△H=-2834.9kJ/mol
4Al(s)+2O3(g)═2Al2O3(s)△H=-3119.91kJ/mol.由此得出的结论正确的是( )
4Al(s)+3O2(g)═2Al2O3(s)△H=-2834.9kJ/mol
4Al(s)+2O3(g)═2Al2O3(s)△H=-3119.91kJ/mol.由此得出的结论正确的是( )
| A、等质量的O2比O3能量低,由O2变O3为放热反应 |
| B、等质量的O2比O3能量低,由O2变O3为吸热反应 |
| C、3O2(g)=2O3(g)△H=285.0kJ/mol |
| D、O3比O2稳定,由O2变O3为吸热反应 |
下列叙述不正确的是( )
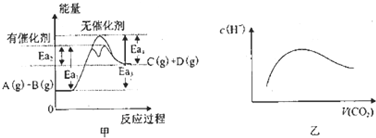

| A、由甲可知,A与B在有催化剂存在的热化学方程式为:A(g)+B(g)?C(g)+D(g)△H═+(Ea3-Ea4)KJ?mol-1 | ||||
B、常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图乙变化关系;当
| ||||
| C、己知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为5.6×10-5mol/L,则生成沉淀所需Na2CO3溶液的最小浓度为2×10-4mol/L | ||||
| D、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混台后(不考虑混台后溶液体积的变化)恰好完全反应,反应后的溶掖中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.05mol?L-1 |
下列溶液中,不能鉴别SO2与CO2气体的是( )
①KMnO4溶液;②H2S;③澄清石灰水;④酸化Ba(NO3)2;⑤FeCl3和BaCl2混合溶液;⑥品红溶液;⑦Na2SiO3溶液;⑧BaCl2溶液.
①KMnO4溶液;②H2S;③澄清石灰水;④酸化Ba(NO3)2;⑤FeCl3和BaCl2混合溶液;⑥品红溶液;⑦Na2SiO3溶液;⑧BaCl2溶液.
| A、③⑦⑧ | B、①②③ |
| C、③④⑤⑦ | D、④⑤⑥⑦ |
将11.2gFe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到40g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在密闭容器中高温加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
| A、2240mL |
| B、4480mL |
| C、3360mL |
| D、1120mL |
已知短周期元素的离子aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系正确的是( )
| A、质子数c>b |
| B、原子半径X<W |
| C、氢化物的稳定性H2Y>HZ |
| D、离子的还原性Y2->Z- |