题目内容
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍.下列说法中不正确的是( )
| A、W、M的某种单质可作为水处理中的消毒剂 |
| B、电解YW2的熔融物可制得Y和W的单质 |
| C、相同条件下,W的氢化物水溶液酸性比Z弱 |
| D、X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、M五种短周期元素,Z、M同主族,结合原子序数可知,Z处于第二周期、M处于第三周期,再由X+与M2-具有相同的电子层结构,可推知M为O元素、X为Na元素;X、Y、Z、W同周期,即均处于第三周期,Y的内层电子总数是最外层电子数的5倍,最外层电子数为2,故Y为Mg,而离子半径:Z2->W-,由离子所带电荷可知,Z为S元素、W为Cl元素,据此解答.
解答:
解:X、Y、Z、W、M五种短周期元素,Z、M同主族,结合原子序数可知,Z处于第二周期、M处于第三周期,再由X+与M2-具有相同的电子层结构,可推知M为O元素、X为Na元素;X、Y、Z、W同周期,即均处于第三周期,Y的内层电子总数是最外层电子数的5倍,最外层电子数为2,故Y为Mg,而离子半径:Z2->W-,由离子所带电荷可知,Z为S元素、W为Cl元素,
A.Cl2和O3都具有强氧化性,则可以作为消毒剂,故A正确;
B.电解熔融MgCl2可制得Mg和氯气,故B正确;
C.HCl溶液比H2S水溶液酸性强,故C错误;
D.Na、O两种元素形成过氧化钠与水反应可以生成氧气,故D正确,
故选C.
A.Cl2和O3都具有强氧化性,则可以作为消毒剂,故A正确;
B.电解熔融MgCl2可制得Mg和氯气,故B正确;
C.HCl溶液比H2S水溶液酸性强,故C错误;
D.Na、O两种元素形成过氧化钠与水反应可以生成氧气,故D正确,
故选C.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固.

练习册系列答案
相关题目
液态化合物AB会发生微弱的自身电离,电离方程式为AB?A++B-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14.则下列叙述正确的是( )
| A、AB的电离是吸热过程 |
| B、在35℃时,c(A+)>c(B-) |
| C、AB的电离程度(25℃)>(35℃) |
| D、c(A+)随温度升高而降低 |
有Fe2+、NO3-、Fe3+、NH4+、H+、H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
| A、氧化剂中心原子的杂化方式为sp2 |
| B、还原剂的外围电子排布式为3d54s1 |
| C、还原产物的VSEPR模型为正四面体 |
| D、该反应可设计为原电池,其负极反应为Fe2+-e-=Fe3+ |
鉴别二甲醚和乙醇可采用化学方法或物理方法,下列方法不能对二者进行鉴别的是( )
| A、利用金属钠或金属钾法 |
| B、利用红外光谱法 |
| C、利用质谱法 |
| D、利用核磁共振氢谱法 |
常温下列各组离子在指定溶液中可能大量共存的是( )
| A、含有大量ClO-的溶液:Na+、OH-、I-、SO32- |
| B、澄清透明的溶液:Cu2+、Fe3+、NO3-、Cl- |
| C、使pH试纸变蓝的溶液:NH4+、K+、S2-、CO32- |
D、c(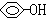 )=0.1mol/L的溶液:Na+、Cl-、CO32-、NO3- )=0.1mol/L的溶液:Na+、Cl-、CO32-、NO3- |
下列物质中各含有少量杂质,能用饱和Na2CO3溶液并借助于分液漏斗除去杂质的是( )
| A、苯中含有少量甲苯 |
| B、乙醇中含少量乙酸 |
| C、乙酸乙酯中含有少量乙酸 |
| D、溴苯中含有少量苯 |
如图是CO2电催化还原为CH4的工作原理示意图.下列说法不正确的是( )
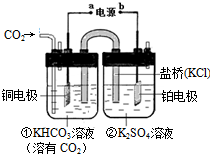

| A、该过程是电能转化为化学能的过程 |
| B、铜电极的电极反应式为CO2+8H++8e-═CH4+2H2O |
| C、一段时间后,①池中n(KHCO3)不变 |
| D、一段时间后,②池中溶液的pH一定下降 |
化学来源于生活,应用于生活,渗透在生活的各个领域.下列有关物质的性质与应用的说法不相对应的是( )
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、FeCl3溶液能与铜反应,可用于蚀刻印刷电路板 |
| C、碳酸氢钠可与盐酸反应,可用作抗酸药 |
| D、SiO2具有良好的导电性,可用作光导纤维 |