题目内容
6.某溶液中Cl-、Br-、I-个数比为1:2:5,欲使这些离子个数比为5:2:1,那么要通入Cl2分子个数与原溶液中I-个数比应为( )| A. | 1:2 | B. | 2:1 | C. | 2:5 | D. | 5:2 |
分析 还原性:I->Br->Cl-,通入一定量的Cl2,比值变为5:2:1,说明溶液中剩余I-,则只氧化I-,Br-的物质的量不变,假定Br-为2mol,根据离子物质的量变化计算通入的氯气的物质的量,以此解答该题.
解答 解:还原性:I->Br->Cl-,通入一定量的Cl2,比值变为5:2:1,说明溶液中剩余I-,
设Cl-、Br-、I-三者物质的量分别是1mol、2mol、5mol,则反应后分别为5mol、2mol、1mol,则增加Cl-4mol,I-减少4mol,
由方程式2I-+Cl2=I2+2Cl-可知,参加反应的Cl2为2mol,
则通入Cl2的分子数与原溶液中I-离子数之比为2mol:5mol=2:5,
故选C.
点评 本题考查卤素单质及其化合物的性质、化学计算等,难度不大,注意比较物质的氧化性、还原性的强弱,根据所发生的反应结合化学方程式计算.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
5.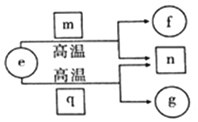 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小:W>Z>X | |
| B. | 简单氢化物的沸点:W>Y>Z | |
| C. | 元素Y、Z、W形成的单质不止一种 | |
| D. | 元素Y、Z、W与元素X均能形成18e-的分子 |
1.一定条件下,对反应C(s)+CO2(g)?2CO(g)△H>0分别进行下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量.上述措施中一定能使反应速率显著加快的是( )
| A. | ①②③ | B. | ①③④ | C. | ①② | D. | ①③ |
11.下列有关化学反应方向及其判据的说法中错误的是( )
| A. | 1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | |
| B. | 凡是放热反应都是自发的,因为吸热反应都是非自发的 | |
| C. | CaCO3(s)?CaO(s)+CO2(g)△H>0 能否自发进行与温度有关 | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
18.下列关于NaHCO3的说法正确的是( )
| A. | 俗名是苏打或纯碱 | B. | 同温度时的溶解度比Na2CO3大 | ||
| C. | 与盐酸反应时比Na2CO3快 | D. | 热稳定性强,受热难以分解 |
15. 在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
 在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
在美化环境时要用到大量盆栽鲜花,为保证鲜花盛开,经常施用S-诱抗素制剂.S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )| A. | 含有碳碳双键、羟基、羰基、羧基 | B. | 含有苯基、羟基、羰基、羧基 | ||
| C. | 含有羟基、羰基、羧基、酯基 | D. | 含有碳碳双键、苯基、羟基、羰基 |
16.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族.下列说法正确的是( )
| A. | 元素Y、W的简单阴离子具有相同的电子层结构 | |
| B. | 由X、W两种元素组成的化合物是离子化合物 | |
| C. | X的简单气态氢化物的热稳定性比W的弱 | |
| D. | 离子半径:r(Z)<r(Y)<r(X)<r(W) |
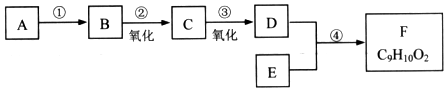
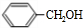 ;
;