题目内容
18.下列关于NaHCO3的说法正确的是( )| A. | 俗名是苏打或纯碱 | B. | 同温度时的溶解度比Na2CO3大 | ||
| C. | 与盐酸反应时比Na2CO3快 | D. | 热稳定性强,受热难以分解 |
分析 A.NaHCO3的俗名是小苏打;
B.Na2CO3比NaHCO3易溶于水;
C.碳酸钠和盐酸反应先生成碳酸氢钠,碳酸氢钠再和盐酸反应生成二氧化碳;
D.NaHCO3不稳定,加热易分解.
解答 解:A.Na2CO3俗名是苏打或纯碱,NaHCO3的俗名是小苏打,故A错误;
B.在饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,说明Na2CO3比NaHCO3易溶于水,则同温度时的溶解度比Na2CO3小,故B错误;
C.碳酸钠和盐酸反应先生成碳酸氢钠,碳酸氢钠再和盐酸反应生成二氧化碳,所以和盐酸反应的快慢:Na2CO3<NaHCO3,故C正确;
D.NaHCO3不稳定,加热易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,故D错误.
故选C.
点评 本题考查Na2CO3和NaHCO3性质的异同,题目难度不大,注意把握Na2CO3和NaHCO3性质,注重基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列关于有机物的叙述不正确的是( )
| A. | 鉴别己烷、己烯和乙醇,可用溴水 | |
| B. | 乙烯和植物油均能使溴的四氯化碳溶液褪色,且反应原理相同 | |
| C. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| D. | 1mol分子式为C18H26O5的酯完全水解生成lmol 羧酸和2mol乙醇,该羧酸分子式为C14H18O5 |
9.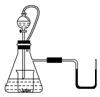 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )| A. | U型管内液体慢慢向右移动说明将分液漏斗中的水滴入到烧杯中一定发生了化学反应 | |
| B. | U型管内液体慢慢向右移动是由于锥形瓶中气体的总物质的量增大造成压强增大而引起 | |
| C. | 该装置中连接分液漏斗和锥形瓶的橡胶管对于上述实验现象而言其实是可有可无的 | |
| D. | 小烧杯中的物质可以是NaOH也可以是Na2O |
6.某溶液中Cl-、Br-、I-个数比为1:2:5,欲使这些离子个数比为5:2:1,那么要通入Cl2分子个数与原溶液中I-个数比应为( )
| A. | 1:2 | B. | 2:1 | C. | 2:5 | D. | 5:2 |
13.核素178O的原子核内的中子数与核外电子数之差是( )
| A. | 9 | B. | 8 | C. | 1 | D. | 17 |
3.德国重离子研究中心2010年2月19日宣布,由该中心人工合成的第ll2号化学元素从即日起获正式名称“Copemicium”,相应的元素符号为“Cn”.该元素的名称是为了纪念著名天文学家哥白尼而得名.该中心人工合成Cn的过程可表示为:7030Zn+20882Pb→277112Cn+10n.下列叙述中正确的是( )
| A. | 上述合成过程属于化学变化 | |
| B. | Cn元素位于元素周期表的第七周期,是副族元素 | |
| C. | Cn元素的相对原子质量为277 | |
| D. | 277112Cn的原子核内质子数比中子数多53 |
7.已知下列反应:NaH+H2O═NaOH+H2↑,在该反应中( )
| A. | NaH是还原剂 | B. | NaH是氧化剂 | ||
| C. | H2O是还原剂 | D. | H2O既不是氧化剂又不是还原剂 |
8.下列说法正确的是( )
| A. | 同周期X、Y、Z元素的最高价含氧酸的酸性:HXO4>H2YO4>H3ZO4,则气态氢化物稳定性HX<H2Y<ZH3 | |
| B. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越弱 | |
| C. | 金属与非金属元素分界线附近的元素是过渡元素 | |
| D. | 元素R的含氧酸的化学式是H2RO3,则其气态氢化物的化学式就是RH4 |

 .
. .
.