题目内容
11.下列离子方程式与所述事实相符且正确的是( )| A. | 实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓ | |
| D. | 向次氯酸钠溶液中通入SO2:2ClO-+SO2+H2O═SO32-+2HClO |
分析 A.氯化氢为强电解质,完全电离;
B.氢氧化钠少量,反应生成碳酸钙、碳酸氢钠和水;
C.二者反应生成硫酸钠、硫酸钡和水;
D.次氯酸根能够氧化亚硫酸根离子.
解答 解:A.实验室用MnO2和浓盐酸制取Cl2,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故A错误;
B.Ca(HCO3)2溶液中加入少量NaOH溶液,离子方程式:Ca2++HCO3-+OH-═CaCO3↓+H2O,故B错误;
C.向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性,离子方程式:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故C正确;
D.向次氯酸钠溶液中通入SO2,离子方程式:2ClO-+SO2+H2O═SO42-+2H++2Cl-,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循客观事实、遵循原子个数守恒,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
相关题目
19.常温下,取0.1mol•L-1 H2X溶液与0.2mol•L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,则下列说法正确的是( )
| A. | c(Na+)=2c(X2-) | B. | c(OH-)=c(H+)+2c(H2X)+c(HX-) | ||
| C. | c(X-)>c(Na+)>c(OH-)>c(H+) | D. | c(Na+)+c(H+)=c(OH-)+c(X2-)+c(HX-) |
6.化学在生产和生活中有重要的应用,下列说法不正确的是( )
| A. | 小苏打在生活中可用做发酵粉 | |
| B. | 过氧化钠可用于呼吸面具中氧气的来源 | |
| C. | 可溶性铁盐或铝盐可用于净水 | |
| D. | 二氧化硅可用于制作硅芯片和光电池 |
3.室温下,向10mL 0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是( )
| A. | 溶液中粒子的数目减小 | |
| B. | 再加入CH3COONa固体能促进醋酸的电离 | |
| C. | 稀释醋酸溶液,溶液中所有离子的浓度均降低 | |
| D. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 |
20.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾与水反应成的Al(OH)3胶体能吸附水中悬浮物,可用于净水 | |
| B. | 江河入海口三角洲的形成通常与胶体的性质有关系 | |
| C. | 水泥厂、冶金厂用高压电作用于气溶胶以除去烟尘,是利用了电泳原理 | |
| D. | 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸 |
1.下列反应的离子方程式正确的是( )
| A. | 铁和稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙溶于稀盐酸中 CO32-+2H+═CO2↑+H2O | |
| C. | 碳酸氢钠溶液与盐酸反应 HCO3-+H+═CO2↑+H2O | |
| D. | 氧化铜与盐酸反应 O2-+2H+═H2O |
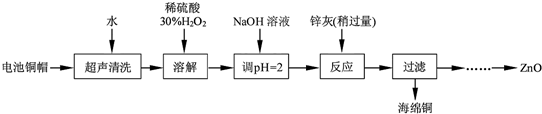
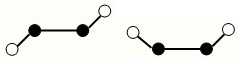
 ,有关该晶体的说法正确的是
,有关该晶体的说法正确的是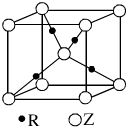
 制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题
制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题