题目内容
下列各物质:①3.01×1023个CH4②标况44.8L C02③17gNH3的物质的量由多到少的顺序是( )
| A、②③① | B、②①③ |
| C、①②③ | D、③②① |
考点:物质的量的相关计算
专题:计算题
分析:结合n=
=
=
计算物质的量,以此来解答.
| N |
| NA |
| V |
| Vm |
| m |
| M |
解答:
解:①3.01×1023个CH4,n(CH4)=
=0.5mol;
②标况44.8L C02,n(C02)=
=2mol;
③17gNH3,n(NH3)=
=1mol,
则物质的量由多到少的顺序是②③①,
故选A.
| 3.01×1023 |
| 6.02×1023 |
②标况44.8L C02,n(C02)=
| 44.8L |
| 22.4L/mol |
③17gNH3,n(NH3)=
| 17g |
| 17g/mol |
则物质的量由多到少的顺序是②③①,
故选A.
点评:本题考查物质的量的计算,为高频考点,把握物质的量、质量、体积的关系及基本计算公式为解答的关键,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知25℃时有关弱酸的电离平衡常数:
由此可得出( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A、对应钠盐溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| B、CO2通入NaCN溶液中有:CO2+H2O+2NaCN→Na2CO3+2HCN |
| C、冰醋酸中逐滴加水,溶液的导电性、pH均先增大后减小 |
| D、NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
足量铜与一定量浓硝酸反应得到Cu(NO3)2溶液和NO2、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得Cu(NO3)2溶液中加入5mol?L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60 mL |
| B、45 mL |
| C、30 mL |
| D、15 mL |
下列各种溶液中,粒子物质的量浓度关系正确的是( )
| A、草酸氢钾溶液呈酸性,0.1mol/LKHC2O4:c(H2C2O4)>c(C2O42-) |
| B、0.2mol?L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C、0.1mol?L-1(NH4)2SO4溶液:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、0.2mol?L-1NaHCO3溶液:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
下列说法不正确的是( )
| A、化学变化一定伴随着能量变化,伴随能量变化的过程未必是化学变化 |
| B、凡是有化学键断裂或形成的变化不一定是化学反应 |
| C、在光照下CH4与Cl2反应时,每一个Cl2分子可取代2个H原子 |
| D、放热反应必定是反应物的总能量>生成物的总能量 |
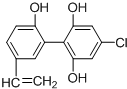 在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )
在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )| A、X分子中不可能所有原子都在同一平面上 |
| B、X遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色 |
| C、1mol X与足量的浓溴水反应,最多消耗5mol Br2 |
| D、1mol X在一定条件下与足量的氢气反应,最多消耗1mol H2 |
下列微粒中:①13Al3+;② ;③
;③ ;④O2-,其核外电子数相同的是( )
;④O2-,其核外电子数相同的是( )
 ;③
;③ ;④O2-,其核外电子数相同的是( )
;④O2-,其核外电子数相同的是( )| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
可用来鉴别苯酚溶液、乙酸乙酯、乙苯、庚烯的一组试剂是( )
| A、银氨溶液、溴水 |
| B、酸性高锰酸钾溶液、氯化铁溶液 |
| C、酸性高锰酸钾溶液、溴水 |
| D、氯化铁溶液、溴水 |