题目内容
8.下列各项操作中,产生“先沉淀,然后沉淀又溶解”现象的是( )①向饱和碳酸钠溶液中通入过量的CO2②向Fe(OH)3胶体中逐滴加入过量的稀硫酸 ③向澄清石灰水溶液中通入过量的CO2④向AlCl3溶液中逐滴加入过量的氢氧化钠溶液.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
分析 ①反应生成碳酸氢钠,相同条件下碳酸钠的溶解度大于碳酸氢钠;
②先发生胶体聚沉,后氢氧化铁沉淀与稀硫酸反应;
③先反应生成碳酸钙,后反应生成碳酸氢钙;
④先生成氢氧化铝沉淀,后氢氧化铝与NaOH反应生成偏铝酸钠和水.
解答 解:①反应生成碳酸氢钠,相同条件下碳酸钠的溶解度大于碳酸氢钠,则观察到沉淀析出,不会溶解,故不选;
②先发生胶体聚沉,后氢氧化铁沉淀与稀硫酸反应,则观察到“先沉淀,然后沉淀又溶解”,故选;
③先反应生成碳酸钙,后反应生成碳酸氢钙,则观察到“先沉淀,然后沉淀又溶解”,故选;
④先生成氢氧化铝沉淀,后氢氧化铝与NaOH反应生成偏铝酸钠和水,则观察到“先沉淀,然后沉淀又溶解”,故选;
故选D.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.“垃圾是放错了位置的资源”,应该分类回收.生活中废弃的铁锅、铝制易拉罐、铜导线等可以归为一类加以回收,它们属于( )
| A. | 氧化物 | B. | 非金属 | C. | 金属或合金 | D. | 碱 |
20.下列离子方程式中正确的是( )
| A. | 碳酸钙和盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 过量的氯化铁和锌反应,锌溶解:2Fe3++Zn═2Fe2++Zn2+ | |
| C. | 醋酸和苯酚钠溶液的反应: O-+CH3COOH→ O-+CH3COOH→ OH↓+CH3COO- OH↓+CH3COO- | |
| D. | 碳酸氢钠溶液与氯化铝溶液反应:Al3++3HCO3-═Al(HCO3)3↓ |
16.下列除去杂质的方法正确的是( )
| A. | 除去N2中的少量O2:通过灼热的CuO粉末 | |
| B. | 除去CO2中的少量HCl:通入Na2CO3溶液 | |
| C. | 除去KCl溶液中的少量K2CO3:加入适量的盐酸 | |
| D. | 除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
13.胶体区别于其它分散系的本质特征是( )
| A. | 胶体粒子直径在1-100nm之间 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子能穿过滤纸 | D. | 胶体有丁达尔效应 |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 常温常压下,22.4L CO2和SO2混合气体含有2NA个O原子 | |
| C. | 常温常压下,8g CH4的体积为11.2L | |
| D. | 标准状况下,22.4L的H2和CO2混合气体中含有的分子总数为NA |
17.将一定体积的某NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液体积为V2,则下列叙述正确的是( )
| A. | 若V1>V2,则说明HA的酸性比HB的酸性强 | |
| B. | 若V1>V2,则说明HA的酸性比HB的酸性弱 | |
| C. | 因为两种酸溶液的pH相等,故V1一定等于V2 | |
| D. | 若将两种酸溶液等体积混合,混合溶液的pH一定等于2 |
18.下列关于糖类、脂肪和蛋白质的叙述正确的是( )
| A. | 蛋白质溶液遇CuSO4后产生的沉淀能重新溶解 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 植物油不能使溴的四氯化碳溶液褪色 |

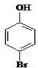 .
. 是化合物 B 的一种同分异构体,用1H 核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境.
是化合物 B 的一种同分异构体,用1H 核磁共振谱可以证明该化合物中有2种氢处于不同的化学环境. .
. .
. .
.