题目内容
19.下列物质中,同压下沸点最高的是( )| A. | HCl | B. | HF | C. | HI | D. | HBr |
分析 同主族元素的氢化物的相对分子质量越大,则熔沸点越高,含有氢键的熔沸点较高,形成氢键数目越多熔沸点越高.
解答 解:同主族元素的氢化物的相对分子质量越大,则熔沸点越高,含有氢键的熔沸点较高,HF、HCl、HBr、HI为第VIⅠA族元素的氢化物,HF分子之间形成氢键,所以四者中HF的熔沸点最高,故选B.
点评 本题考查沸点的比较,明确物质的关系及比较沸点的方法即可解答,难度不大,注意氢键对物质物理性质的影响.

练习册系列答案
相关题目
9.(NH4)2Fe(SO4)2•6H2O(莫尔盐,浅绿色,式量392)在定量分析中常用作标定高锰酸钾、重铬酸钾等溶液的标准物质,还用化学试剂、医药以及用于冶金、电镀等.回答下列问题:
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置在空气中也会变质,检验莫尔盐是否变质的试剂是KSCN溶液.
(2)准确称取mg纯净的莫尔盐,在锥形瓶中加入20mL水充分溶解,用某酸性K2Cr2O7溶液滴定至终点.重复进行3次,测得有关数据如表:
①K2Cr2O7溶液应该放在酸式滴定管中.
②写出滴定过程中反应的离子方程式6Fe2++Cr2O72-+14H+=2Cr3++6Fe3++7H2O.
③所测K2Cr2O7溶液的物质的量浓度为$\frac{m}{47.04}$mol/L(用含m的代数式表示).
(3)某课题组通过实验检验莫尔盐晶体加热时的分解产物.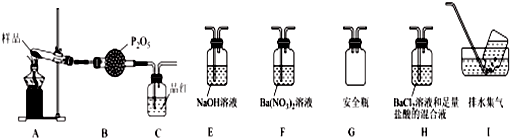
①甲同学提出猜想:分解产物可能是N2、Fe2O3、SO2、H2O四种物质.你是否同意并说明理由:不同意,N、Fe的化合价均升高,没有化合价降低的元素.
②乙同学设计了如图装置,其中A装置中的固体变为红棕色,则固体产物中含有Fe2O3;C装置中红色褪去,说明气体产物中含有SO2;C装置后应连接尾气吸收装置D,D中盛有的试剂可以是NaOH溶液(写一种即可).
③丙同学想利用上述装置证明分解产物中含有氨气,只需更换B、C中的试剂即可,则更换后的试剂为B碱石灰,C酚酞溶液.
④丁同学认为莫尔盐分解可能会生成N2、SO2,拟从下列装置中选择必要的装置加以证明,则正确的连接顺序从左到右依次是A、G、H、I.
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置在空气中也会变质,检验莫尔盐是否变质的试剂是KSCN溶液.
(2)准确称取mg纯净的莫尔盐,在锥形瓶中加入20mL水充分溶解,用某酸性K2Cr2O7溶液滴定至终点.重复进行3次,测得有关数据如表:
| 实验序号 | 起始读数/mL | 终点读数/mL |
| Ⅰ | 2.50 | 22.58 |
| Ⅱ | 1.00 | 23.42 |
| Ⅲ | 0.00 | 19.92 |
②写出滴定过程中反应的离子方程式6Fe2++Cr2O72-+14H+=2Cr3++6Fe3++7H2O.
③所测K2Cr2O7溶液的物质的量浓度为$\frac{m}{47.04}$mol/L(用含m的代数式表示).
(3)某课题组通过实验检验莫尔盐晶体加热时的分解产物.

①甲同学提出猜想:分解产物可能是N2、Fe2O3、SO2、H2O四种物质.你是否同意并说明理由:不同意,N、Fe的化合价均升高,没有化合价降低的元素.
②乙同学设计了如图装置,其中A装置中的固体变为红棕色,则固体产物中含有Fe2O3;C装置中红色褪去,说明气体产物中含有SO2;C装置后应连接尾气吸收装置D,D中盛有的试剂可以是NaOH溶液(写一种即可).
③丙同学想利用上述装置证明分解产物中含有氨气,只需更换B、C中的试剂即可,则更换后的试剂为B碱石灰,C酚酞溶液.
④丁同学认为莫尔盐分解可能会生成N2、SO2,拟从下列装置中选择必要的装置加以证明,则正确的连接顺序从左到右依次是A、G、H、I.
7.下列事实中,不能说明HR是弱酸的是( )
| A. | 0.1mol/L HR溶液与0.1mol/L氨水等体积反应,所得溶液呈酸性 | |
| B. | NaR晶体用蒸馏水配成水溶液,PH试纸测得PH大于7 | |
| C. | 将PH=2.3的HR溶液加蒸馏水稀释10倍,PH变成2.8 | |
| D. | 常温下,0.1mol/L HR溶液的pH为2 |
14.下列说法中不正确的是( )
| A. | 往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘 | |
| B. | 通常用产生气泡的快慢,比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 | |
| C. | 在“催化剂对过氧化氢分解反应速率的影响”实验中,MnO2的用量以及颗粒直径的大小均会影响H2O2分解的速率,溶液的酸碱性对H2O2的稳定性也有较大的影响 | |
| D. | 在适量氯化钴的乙醇溶液中,逐滴加入水至溶液恰好呈粉红色,加热该溶液,结果依次呈现紫色、蓝紫色、蓝色的变化 |
4.对于反应2SO2(g)+O2(g)?2SO3(g),一次只改变一个条件,能增大逆反应速率的措施是( )
| A. | 增大容器体积 | B. | 通入大量O2 | C. | 移去部分SO2 | D. | 降低体系温度 |
11.下列过程中不涉及化学变化的是( )
| A. | 粮食酿酒 | B. | 用食醋除去水壶中的水垢 | ||
| C. | 用木炭除去冰箱中的异味 | D. | 苹果腐烂 |
5.下列有机物不属于烃的衍生物的是( )
| A. | CH2=CHCl | B. | CH2=CH2 | C. | CH3CH2NO2 | D. | CCl4 |