题目内容
18.某化学反应,设反应物总能量为E1,生成物总能量为E2,且E1<E2,则该反应是(请填放热或吸热)吸热反应.分析 反应物总能量大于生成物总能量,反应是放热反应,反应物总能量小于生成物总能量,反应是吸热反应,据此回答.
解答 解:反应物总能量大于生成物总能量,反应是放热反应,反应物总能量小于生成物总能量,反应是吸热反应,故答案为:吸热.
点评 本题考查学生反应吸热还是放热的判断方法,注意能量守恒思想在结论的记忆中的作用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列反应属于吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 生石灰与水的反应 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
13.离子键和共价键可能同时存在于同一化合物中.下列化合物中既存在离子键又存在共价键的是( )
| A. | KBr | B. | Na2O | C. | HBr | D. | NH4NO3 |
10.现将等物质的量的CuSO4、FeCl3、Zn放入盛有水的烧杯中充分反应,所得溶液中除SO42-、Cl-外,还含有的金属阳离子是( )
| A. | Zn2+、Cu2+、Fe3+ | B. | Zn2+、Cu2+、Fe2+ | ||
| C. | Zn2+、Fe2+、Cu2+、Fe3+ | D. | Zn2+、Fe3+ |
9.有下列八种物质:①氯化钙、②金刚石、③硫、④氢氧化钠、⑤二氧化硅、⑥干冰,回答有关这八种物质的问题.(用编号回答)
(1)将这八种物质按不同晶体类型分成四组,并填写下表:
(2)属于共价化合物的是⑤⑥;含有共价键的离子化合物是④;
(3)其中硬度最大的物质是②;熔点最低的物质是⑥.
(1)将这八种物质按不同晶体类型分成四组,并填写下表:
| 晶体类型 | 离子晶体 | 原子晶体 | 分子晶体 |
| 各组中物质的编号 | ①④ | ②⑤ | ③⑥ |
(3)其中硬度最大的物质是②;熔点最低的物质是⑥.


 .
. 同分异构体有4种.
同分异构体有4种. 的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:
的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例: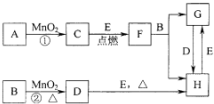 图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物.它们存在如下转化关系,反应中生成的水及次要产物均已略去.
图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物.它们存在如下转化关系,反应中生成的水及次要产物均已略去.