题目内容
3.甲烷的电子式为 ,碳氢键之间键角为109°28′.甲烷和氯气在光照下发生取代反应,生成5种产物.产物中CCl4常用作灭火剂.试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.
,碳氢键之间键角为109°28′.甲烷和氯气在光照下发生取代反应,生成5种产物.产物中CCl4常用作灭火剂.试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.
分析 1个甲烷分子中含1个C、4个H原子,碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,为正四面体;
甲烷和氯气光照发生取代反应,反应是连锁反应,生成产物为一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳、氯化氢五种物质,其中四氯化碳不支持燃烧,四氯化碳比空气重,覆盖在燃烧物表面,以阻止氧气的进入,具有灭火的作用;
三溴甲烷在光照条件下与溴蒸气发生取代反应生成四溴甲烷和溴化氢,据此书写方程式.
解答 解:1个甲烷分子中含1个C、4个H原子,碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,电子式: ;
;
甲烷为正四面体积结构,碳氢键之间键角为:109°28′;
烷和氯气光照发生取代反应,反应是连锁反应,生成产物为一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳、氯化氢五种物质;
其中四氯化碳不支持燃烧,四氯化碳比空气重,覆盖在燃烧物表面,以阻止氧气的进入,具有灭火的作用;
三溴甲烷在光照条件下与溴蒸气发生取代反应生成四溴甲烷和溴化氢,化学方程式:CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr;
故答案为: ;109°28′;5;CCl4;CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.
;109°28′;5;CCl4;CHBr3+Br2$\stackrel{光照}{→}$CBr4+HBr.
点评 本题考查了有机物结构特点及性质,明确甲烷的结构及化学性质是解题关键,注意烷烃取代反应条件为光照,注意甲烷的正四面体积结构特点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.1-乙炔基-1-环己醇可用作加成型硅橡胶储存稳定剂、硅氢加成反应抑制剂,还可用作油墨、油漆以及涂料的催干剂等,其结构如图所示: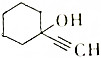 将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮(
将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮( 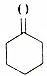 ),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )
),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )
 将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮(
将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮(  ),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )
),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )| A. | 1:1 | B. | 1:2 | C. | 13:49 | D. | 24:49 |
14.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.
供选择的化学试剂及实验方法A.将气体通入盛有NaOH溶液的洗气瓶B.取样,滴加KSCN溶液C.取样,滴加酚酞试液D.取样,灼烧.
| 实验 目 的 | 试剂及方法 |
| 鉴别丝绸和棉布 | |
| 除去CO中混有少量CO2 | |
| 证明Na2CO3溶液呈碱性 | |
| 检验溶液中是否含Fe3+ |
11.下列关于烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键;
②烷烃中除甲烷外,很多都能使高锰酸钾溶液的紫色褪去;
③分子通式为CnH2n+2的烃不一定是烷烃;
④所有的烷烃在光照条件下都能与氯气发生取代反应;
⑤光照条件下,乙烷通入氯水中,可使氯水褪色.
①在烷烃分子中,所有的化学键都是单键;
②烷烃中除甲烷外,很多都能使高锰酸钾溶液的紫色褪去;
③分子通式为CnH2n+2的烃不一定是烷烃;
④所有的烷烃在光照条件下都能与氯气发生取代反应;
⑤光照条件下,乙烷通入氯水中,可使氯水褪色.
| A. | ①③⑤ | B. | ②③ | C. | ①④ | D. | ①②④ |
18.下列说法正确的是( )
| A. | 共价化合物中一定不含离子键 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 任何化学物质中均存在化学键 | |
| D. | 全部由非金属元素形成的化合物一定是共价化合物 |
8.下列有关如图所示原电池装置描述正确的是( )
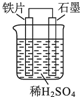

| A. | 石墨电极作负极 | |
| B. | 铁片上的反应:Fe-2e-=Fe2+ | |
| C. | 铁电极附近溶液中氢离子浓度增大 | |
| D. | 电子由石墨电极通过导线流向铁电极 |
12.一个外围电子构型为2s22p5的元素,下列有关它的描述正确的有( )
| A. | 原子序数为7 | B. | 周期表中第一电离能最小 | ||
| C. | 周期表中原子半径最大 | D. | 周期表中电负性最大 |
13.苯环结构中不存在碳碳双键,而是一种介于单键和双键之间的结构,下列不可以作为事实依据的是( )
| A. | 苯不能使酸性KMnO4溶液褪色 | |
| B. | 苯不能使溴水因发生化学反应而褪色 | |
| C. | 苯在加热和有催化剂存在条件下与H2反应生成环己烷 | |
| D. | 邻二氯苯只有一种结构 |
