题目内容
把氢气和氮气以1:1的物质的量之比放入一容积固定的容器中,温度不变时测得平衡时氮气的转化率为20%时,求:
(1)反应前后的压强之比?
(2)平衡时混合体系的平均摩尔质量?
(1)反应前后的压强之比?
(2)平衡时混合体系的平均摩尔质量?
考点:化学平衡的计算
专题:化学平衡专题
分析:设起始时氮气的物质的量为xmol,则氢气也为xmol,
N2 +3H2 ?2NH3,
开始(mol):x x 0
变化(mol):0.2x 0.6x 0.4x
平衡(mol):x-0.2x x-0.6x 0.4x
结合数据列方程求解;
N2 +3H2 ?2NH3,
开始(mol):x x 0
变化(mol):0.2x 0.6x 0.4x
平衡(mol):x-0.2x x-0.6x 0.4x
结合数据列方程求解;
解答:
解:设起始时氮气的物质的量为xmol,则氢气也为xmol,
N2 +3H2 ?2NH3,
开始(mol):x x 0
变化(mol):0.2x 0.6x 0.4x
平衡(mol):x-0.2x x-0.6x 0.4x
(1)恒温恒压,反应前后的压强之比等于物质的量之比,所以反应前后的压强之比=
=5:4,
答:反应前后的压强之比5:4;
(2)平衡时混合体系的平均摩尔质量=
=
=
=18.75g/mol,
答:平衡时混合体系的平均摩尔质量18.75g/mol;
N2 +3H2 ?2NH3,
开始(mol):x x 0
变化(mol):0.2x 0.6x 0.4x
平衡(mol):x-0.2x x-0.6x 0.4x
(1)恒温恒压,反应前后的压强之比等于物质的量之比,所以反应前后的压强之比=
| 2x |
| 0.8x+0.4x+0.4x |
答:反应前后的压强之比5:4;
(2)平衡时混合体系的平均摩尔质量=
| m 总 |
| n 总 |
| 28x+2x |
| 0.8x+0.4x+0.4x |
| 30 |
| 1.6 |
答:平衡时混合体系的平均摩尔质量18.75g/mol;
点评:考查化学平衡的有关计算,难度不大,掌握平衡计算三段式解题法.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
一定温度下,在一个容积为1L的密闭容器中,充入1mol H2(g)和1mol I2(g),发生反应H2(g)+I2(g)?2HI(g),经充分反应达到平衡后,生成的HI(g)的气体体积的50%,在该温度下,在另一个容积为2L的密闭容器中充入1mol HI(g)发生反应HI(g)?
H2(g)+
I2(g),则下列判断正确的是( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、后一反应的平衡常数为1 |
| B、后一反应的平衡常数为0.5 |
| C、后一反应达到平衡时,H2的平衡浓度为0.25mol?L-1 |
| D、后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol?L-1 |
反应2A(气)+3B(气)?xC(气)+yD(气),已知起始浓度A为5mol/L,B为3mol/L;C的反应速率为0.5mol/L?min;反应开始至平衡需2min;平衡时D的浓度为0.5mol/L.下列说法不正确的是( )
| A、V(A)平:V(B)平=5:3 |
| B、A的转化率为20% |
| C、x:y=2:1 |
| D、D的反应速率为0.25 mol/(L?min) |
满足通式CnH2nO的有机物甲,既可被氧化为一元羧酸乙,又可被还原为一元醇丙,乙和丙在一定条件下反应生成酯丁,则下列说法正确的是( )
| A、甲和丁的最简式相同 |
| B、丁的分子量是丙的两倍 |
| C、甲既可是饱和一元醛,又可是饱和一元酮 |
| D、甲的分子中一定具有甲基 |
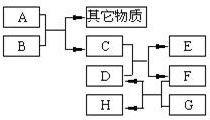 已知B为黑色粉末,用D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示.
已知B为黑色粉末,用D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示.