题目内容
下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)金属性最强的元素是 (填元素名称);
(2)Ar原子结构示意图为 ;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是 (填化学式);
(4)C和N中,原子半径较小的是 ;
(5)“高钙牛奶”中的钙是指 (填“元素”或“单质”);
(6)MgO和Al2O3中,属于两性氧化物的是 .
| 主族 周期 | IA | IIA | IIIA | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)Ar原子结构示意图为
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是
(4)C和N中,原子半径较小的是
(5)“高钙牛奶”中的钙是指
(6)MgO和Al2O3中,属于两性氧化物的是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)根据金属元素活动顺序进行分析;
(2)Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(3)非金属性越强,最高价氧化物对应水化物酸性越强;
(4)同周期自左而右原子半径减小;
(5)“高钙牛奶”中的钙元素以化合态形式存在;
(6)氧化铝能与强酸、强碱反应生成相应的盐与水,属于两性氧化物.
(2)Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(3)非金属性越强,最高价氧化物对应水化物酸性越强;
(4)同周期自左而右原子半径减小;
(5)“高钙牛奶”中的钙元素以化合态形式存在;
(6)氧化铝能与强酸、强碱反应生成相应的盐与水,属于两性氧化物.
解答:
解:(1)表中3种金属中,再金属元素活动顺序中由强到弱顺序为Ca、Na、Mg,故钙的金属性最强,故答案为:钙;
(2)Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8,原子结构示意图为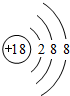 ,故答案为:
,故答案为: ;
;
(3)非金属性越强,最高价氧化物对应水化物酸性越强,第3周期元素中,Cl元素非金属性最强,故HClO4的酸性最强,故答案为:HClO4;
(4)同周期自左而右原子半径减小,故原子半径C>N,故答案为:N;
(5)“高钙牛奶”中的钙元素以化合态形式存在,“高钙牛奶”中的钙是指元素,故答案为:元素;
(6)氧化镁能与酸反应,不能与碱反应,不属于两性氧化物,而氧化铝能与强酸、强碱反应生成相应的盐与水,属于两性氧化物,故答案为:Al2O3.
(2)Ar原子核外有18个电子,有3个电子层,各层电子数为2、8、8,原子结构示意图为
 ,故答案为:
,故答案为: ;
;(3)非金属性越强,最高价氧化物对应水化物酸性越强,第3周期元素中,Cl元素非金属性最强,故HClO4的酸性最强,故答案为:HClO4;
(4)同周期自左而右原子半径减小,故原子半径C>N,故答案为:N;
(5)“高钙牛奶”中的钙元素以化合态形式存在,“高钙牛奶”中的钙是指元素,故答案为:元素;
(6)氧化镁能与酸反应,不能与碱反应,不属于两性氧化物,而氧化铝能与强酸、强碱反应生成相应的盐与水,属于两性氧化物,故答案为:Al2O3.
点评:本题考查元素周期律、原子结构示意图、元素化合物性质等,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
下列化学反应的离子方程式正确的是( )
(1)向CH2ClCOOH中加入足量的氢氧化钠溶液并加热:CH2ClCOOH+OH-
CH2ClCOO-+H2O
(2)在稀氨水中通入过量CO2:NH3?H2O+CO2═NH4++HCO3-
(3)少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
(4)氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
(5)向小苏打溶液中加入过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O
(6)向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
(7)向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH3-+OH-═NH3?H2O
(8)用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑
(1)向CH2ClCOOH中加入足量的氢氧化钠溶液并加热:CH2ClCOOH+OH-
| △ |
(2)在稀氨水中通入过量CO2:NH3?H2O+CO2═NH4++HCO3-
(3)少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
(4)氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
(5)向小苏打溶液中加入过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O
(6)向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
(7)向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH3-+OH-═NH3?H2O
(8)用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑
| A、(2)(3)(5) |
| B、(3)(4)(6) |
| C、(1)(3)(5)(7)(8) |
| D、(2)(5)(6) |
NaHSO4溶于水的过程中,发生变化的化学键有( )
| A、离子键 |
| B、共价键 |
| C、既有离子键又有共价键 |
| D、化学键未发生变化 |
在标准状况下①6.72L CH4②3.01×1023个HCl分子③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达不正确的是( )
| A、体积②>③>①>④ |
| B、密度②>③>④>① |
| C、质量②>③>①>④ |
| D、氢原子个数①>④>③>② |
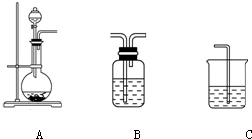 (1)下列实验操作或对实验事实的描述正确的有
(1)下列实验操作或对实验事实的描述正确的有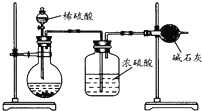 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案: