题目内容
3.下列电离方程式中,不正确的是( )| A. | HCl═H++Cl- | B. | H2SO4═2H++SO42- | C. | FeCl3═Fe3++Cl- | D. | NaOH═Na++OH- |
分析 明确电解质强弱,强电解质完全电离,用等号,弱电解质部分电离,应可逆号,注意电离方程式遵循原子个数、电荷数守恒规律,据此解答.
解答 解:A.氯化氢为强电解质,完全电离,电离方程式:HCl═H++Cl-,故A正确;
B.硫酸强电解质,完全电离,电离方程式:H2SO4═2H++SO42-,故B正确;
C.氯化铁为强电解质,完全电离,电离方程式:FeCl3═Fe3++3Cl-,故C错误;
D.氢氧化钠为强电解质,完全电离,电离方程式:NaOH═Na++OH-,故D正确;
故选:C.
点评 本题考查了电解质电离方程式的书写,明确电解质类型及电离方式是解题关键,注意电离方程式遵循客观事实、遵循原子个数守恒、电荷守恒规律,题目难度不大.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
13.对于反应:M+N-→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到40℃时,完成反应的10%需要的时间为( )
| A. | 9 min | B. | 27 min | C. | 13.5 min | D. | 3 min |
14.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为2NA | |
| B. | 在反应KClO3+6HCl═KCl+3Cl2+3H2O中,每生成3molCl2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为2NA | |
| D. | 某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO3分子数为0.2NA |
11.将一小块金属钠投入下列溶液中,既能产生气体又会出现白色沉淀的是( )
| A. | 稀硫酸 | B. | 硫酸铜溶液 | C. | 稀氢氧化钠溶液 | D. | 氯化镁溶液 |
18.下列说法正确的是( )
| A. | 在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ/mol | |
| B. | 在101 kPa时,1 mol H2完全燃烧生成水蒸气,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ/mol | |
| C. | 热化学方程式C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol表示1个固态碳原子和1分子水蒸气反应吸热131.1kJ | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,在相同条件下,将含0.5 mol H2SO4的稀硫酸与含1 mol Ba(OH)2的水溶液混合,放出的热量可能大于57.3 kJ |
8.氧化还原反应的实质是( )
| A. | 物质跟氧气反应 | |
| B. | 有氧原子得失的反应 | |
| C. | 有元素化合价升降的反应 | |
| D. | 有电子得失或共用电子对发生偏移的反应 |
15.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使紫色石蕊试剂变红的溶液中:NO3-、I-、Ba2+、Fe2+ | |
| B. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| C. | pH=1的溶液中:K+、Br-、SO42-、Al3+ | |
| D. | 澄清石灰水中:Na+、K+、CH3COO-、HCO3- |
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol?L-1 A1C13溶液中含有的Al3+数目小于NA | |
| B. | 标准状况下,11 g3H216O中含有的质子数目为6NA | |
| C. | 1 mol Li2O和Na2O2的混合物中含有的离子总数大于3NA | |
| D. | 常温常压下,4.6 g NO2所含的氮原子数目为0.1NA |
13.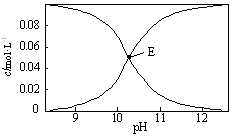 20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )
20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )
 20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )
20℃时,配制一组c(Na2CO3)+c(NaHCO3)=0.100mol•L-1的混合溶液,溶液中c(HCO3-)、c(CO32-)与pH的关系如图所示.下列指定溶液中微粒的物质的量浓度关系正确的是( )| A. | pH=9的溶液中:c(HCO3-)>c(H2CO3)>c(CO32-) | |
| B. | c(HCO3-)=c(CO32-)的E点溶液中:c(OH-)+c(CO32-)>c(H+)+c(H2CO3)+0.050 mol•L-1 | |
| C. | pH=11的溶液中:c(Na+)<2c(CO32-)+c(HCO3-) | |
| D. | 0.100 mol•L-1的Na2CO3溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) |