题目内容
 如图所示,相同温度下,在容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g)?H2(g)+I2(g).下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法正确的是( )
如图所示,相同温度下,在容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g)?H2(g)+I2(g).下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法正确的是( )| A、Ⅰ中活化分子数比Ⅱ中多 |
| B、Ⅰ中活化分子数比Ⅱ中少 |
| C、Ⅰ中活化分子百分数比Ⅱ中少 |
| D、Ⅰ和Ⅱ中活化分子百分数相等 |
考点:化学反应速率的影响因素,化学平衡建立的过程
专题:化学反应速率专题
分析:容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g)?H2(g)+I2(g).由图可知,II的压强大,以此解答.
解答:
解:容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g)?H2(g)+I2(g),由图可知,II的压强大,则II中反应速率大,因该反应为气体体积不变的反应,压强增大,平衡不移动,则正逆反应速率始终相等,Ⅰ和Ⅱ中活化分子百分数相等,
故选D.
故选D.
点评:本题考查影响反应速率的因素,为高频考点,把握反应为气体体积不变的反应为解答的关键,侧重分析能力与知识应用能力的考查,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列化学用语正确的是( )
| A、氮气的电子式N┇┇N |
B、S的结构示意图: |
C、CH4的比例模型: |
| D、二氧化碳的结构式:O-C-O |
下列过程属于化学变化的是( )
| A、煤的干馏 | B、蒸发 |
| C、萃取 | D、蒸馏 |
下列化学用语,应用正确的是( )
A、硝基苯的结构简式是: |
B、乙炔的电子式是: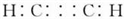 |
C、乙醚分子的球棍模型是: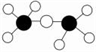 |
| D、甲酸中存在-CHO和-COOH两种官能团 |
下列有关热化学方程式或反应热的说法正确的是( )
A、已知:H2(g)+
| ||||
| B、已知:S(g)+O2(g)═SO2(g)△H1=-Q1 kJ?mol-1;S(s)+O2(g)═SO2(g)△H2=-Q2 kJ?mol-1(Q1、Q2均正值),则Q1<Q2 | ||||
C、已知:
| ||||
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
下列反应中,属于加成反应的是( )
| A、甲烷与氯气混合,光照一段时间后黄绿色消失 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、将苯滴入少量到溴水中,振荡后水层接近无色 |
| D、乙烯使溴水褪色 |
现有C6H6 和C6H6O组成的混合物中,碳的质量分数为a%,则氧的质量分数为( )
A、(1-a%)×
| ||
B、a%×
| ||
| C、1-a% | ||
| D、(1-13a%/12) |
实验室用锌片与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
| A、加入硫酸钾溶液 |
| B、加入几滴硫酸铜溶液 |
| C、改用热的2mol/L硫酸溶液 |
| D、改用浓硫酸溶液 |
有两份质量相同的NaHCO3,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却至原温度再加入相同浓度的盐酸,充分反应,则它们所耗用的盐酸的体积比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、4:1 |