题目内容
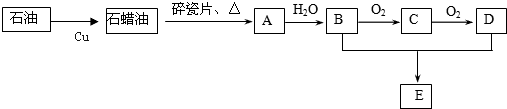
8.有机化合物反应如图1,据此回答下列问题: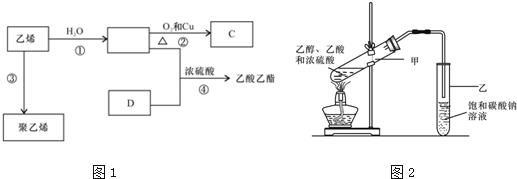
(1)乙烯的结构式为:
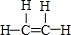 .
.(2)写出反应②④的化学方程式:
②2CH3CH2OH+O2 $→_{△}^{Cu}$ 2CH3CHO+2H2O,反应类型:氧化反应;
④CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O,反应类型:酯化反应或取代反应.
CH3COOCH2CH3+H2O,反应类型:酯化反应或取代反应.(3)实验室常用下列装置制取乙酸乙酯(图2),请回答相关问题:
①饱和碳酸钠溶液的主要作用是除去粗产品中的乙酸、乙醇,酯在其中的溶解度小,有利于酯分离.
②若要把制得的乙酸乙酯分离出来,应采用的操作是分液.
③进行该实验时,最好向试管甲中加入几块碎瓷片,其目的是防暴沸.
分析 乙烯发生加聚反应生成聚乙烯,乙烯与水发生加成反应生成CH3CH2OH,乙醇在Cu作催化剂、加热条件下发生氧化反应生成C为CH3CHO,乙醇与D反应生成乙酸乙酯,则D为CH3COOH.制备乙酸乙酯中,利用饱和的碳酸钠溶液除去产品中的乙酸、乙醇,降低乙酸乙酯溶解度,有利于酯的分层,再用分液的方法分离出乙酸乙酯.
解答 解:乙烯发生加聚反应生成聚乙烯,乙烯与水发生加成反应生成CH3CH2OH,乙醇在Cu作催化剂、加热条件下发生氧化反应生成C为CH3CHO,乙醇与D反应生成乙酸乙酯,则D为CH3COOH.
(1)乙烯的结构式为: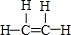 ,故答案为:
,故答案为: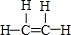 ;
;
(2)反应②的化学方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$ 2CH3CHO+2H2O,属于氧化反应,
反应④的化学方程式为:CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O,属于酯化反应或取代反应,
CH3COOCH2CH3+H2O,属于酯化反应或取代反应,
故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$ 2CH3CHO+2H2O,氧化反应;
CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O,酯化反应或取代反应;
CH3COOCH2CH3+H2O,酯化反应或取代反应;
(3)①乙酸乙酯制备中饱和碳酸钠溶液的主要作用是:除去粗产品中的乙酸、乙醇,酯在其中的溶解度小,有利于酯分离,
故答案为:除去粗产品中的乙酸、乙醇,酯在其中的溶解度小,有利于酯分离;
②若要把制得的乙酸乙酯分离出来,应采用的操作是分液,故答案为:分液;
③乙酸乙酯制备中,最好向试管甲中加入几块碎瓷片,其目的是:防暴沸,故答案为:防暴沸.
点评 本题考查有机物的推断、乙酸乙酯的制备,比较基础,注意乙酸乙酯制备中饱和碳酸钠溶液作用,装置中导管不能伸入液面以下,以防止倒吸.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列颜色变化与氧化还原反应无关的是( )
| A. | 将乙醛加入新制氢氧化铜中加热,出现砖红色沉淀 | |
| B. | 将乙醇滴入酸性重铬酸钾溶液中,溶液由橙色变为绿色 | |
| C. | 将二氧化硫通入滴有酚酞的氢氧化钠溶液中,溶液红色褪去 | |
| D. | 新制氯水敞口久置,颜色褪去 |
19.下列叙述中错误的是( )
| A. | 还原性:Na>Mg>Al>Fe | B. | 碱性:NaOH>KOH>Ca(OH)2 | ||
| C. | 稳定性:HF>HCl>HBr>HI | D. | 酸性:HClO4>H2SO4>CH3COOH>H2CO3 |
16.由苯作原料不能经一步化学反应制得的是( )
| A. | 硝基苯 | B. | 环己烷 | C. | 苯酚 | D. | 溴苯 |
17.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 0.5 mol O3与11.2 L O2所含的分子数一定相等 | |
| C. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压,22.4 L的NO2和CO2混合气体含有2NA个氧原子 |
18.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 中性溶液中:Cl-、Mg2+、Al3+、K+ | |
| B. | 1.0mol•L-1的NaAlO2溶液中:Cl-、HCO3-、K+、Ca2+ | |
| C. | 在强碱性环境中:AlO2-、SiO32-、Na+、K+ | |
| D. | 0.1mol•L-1明矾溶液中:NH4+、AlO2-、HCO3-、Na+ |
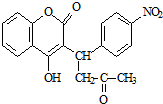 ,醋硝香豆素可以通过以下方法合成(部分反应条件省略).
,醋硝香豆素可以通过以下方法合成(部分反应条件省略).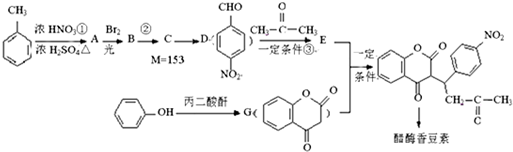
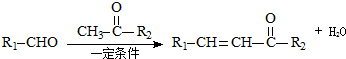
 ;反应②的反应类型水解反应或取代反应.
;反应②的反应类型水解反应或取代反应.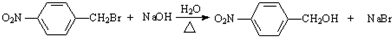 .
.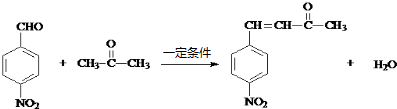 .
.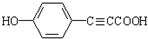 .
.