题目内容
下列描述正确的是( )
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可通过溶液导电能力的大小判断强弱电解质 |
| D、在NaHSO4溶液中存在的离子有:Na+、H+、HSO4-、OH- |
考点:混合物和纯净物,强电解质和弱电解质的概念,离子共存问题
专题:物质的分类专题
分析:A、根据酸、碱、盐、氧化物的概念来回答;
B、根据电解质和非电解质的概念来回答;
C、溶液的导电能力以离子的浓度和电荷有关;
D、在水溶液里,硫酸氢钠电离出氢离子、钠离子和硫酸根离子.
B、根据电解质和非电解质的概念来回答;
C、溶液的导电能力以离子的浓度和电荷有关;
D、在水溶液里,硫酸氢钠电离出氢离子、钠离子和硫酸根离子.
解答:
解:A、纯碱是碳酸钠的俗称,叫碱不是碱,属于盐类,故A错误;
B、蔗糖在水溶液和熔融态下均不导电,属于非电解质,硫酸钡在熔融态时完全电离,属于强电解质,水只能部分电离,属于弱电解质,故B正确;
C、因溶液的导电能力与离子的浓度和电荷有关,强弱电解质与电离程度有关,二者没有必然的联系,故C错误;
D、在水溶液,在水分子的作用下,硫酸氢钠电离出氢离子、钠离子和硫酸根离子,不存在HSO4-,故D错误;
故选B.
B、蔗糖在水溶液和熔融态下均不导电,属于非电解质,硫酸钡在熔融态时完全电离,属于强电解质,水只能部分电离,属于弱电解质,故B正确;
C、因溶液的导电能力与离子的浓度和电荷有关,强弱电解质与电离程度有关,二者没有必然的联系,故C错误;
D、在水溶液,在水分子的作用下,硫酸氢钠电离出氢离子、钠离子和硫酸根离子,不存在HSO4-,故D错误;
故选B.
点评:本题考查知识点较多,但多为基础知识,注重对学生基础知识的考查,明确有关的概念即可解答,较简单.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
要配制下列含有四种不同阴、阳离子的溶液,其中能配制成功的是( )
| A、Fe2+、OH-、NO3-、Cl- |
| B、Ca2+、H+、Cl-、HCO3- |
| C、Mg2+、Al3+、Cl-、SO42- |
| D、Na+、Ca2+、NO3-、CO32- |
下列电离方程式不正确的是( )
| A、Al2 (SO4)3=2Al3++3SO42- |
| B、Ba(OH)2=Ba2++2OH- |
| C、Na2SO4=Na2++SO42- |
| D、NH4NO3=NH4++NO3- |
下列各组物质按酸、碱、盐分类顺序排列正确的是( )
| A、硫酸、纯碱、硝酸钠 |
| B、醋酸、烧碱、明矾[KAl(SO4)2?12H2O] |
| C、硝酸、乙醇、高锰酸钾 |
| D、盐酸、熟石灰、苛性钠 |
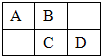 A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.
A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.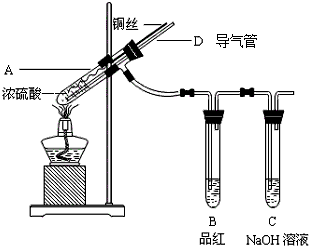 某同学为了探究铜与浓硫酸的反应,进行了如下实验.
某同学为了探究铜与浓硫酸的反应,进行了如下实验.