题目内容
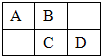 A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.
A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.(1)写出A、B、C、D四种元素符号
(2)D位于元素周期表中第
(3)D的单质与水反应的离子方程式为:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为短周期元素,由它们在周期表中的位置,可知A、B处于第二周期,C、D处于第三周期,令A原子核外电子为x,则B质子数为x+1,C核外电子数为x+9,D核外电子数为x+10,依据题意得出:x+9=2(x+1),解得x=7,故A为N元素、B为O元素、C为S元素,D为C了元素,据此解答各小题即可.
解答:
解:依据分析可知:A、B、C、D分别为:氮、氧、硫、氯,
(1)A、B、C、D分别为:氮、氧、硫、氯,元素符号分别为:N、O、S、Cl,故答案为:N、O、S、Cl;
(2)D为Cl,处于第三周期第VIIA族,故答案为:三;VIIA;
(3)氯气与水反应生成盐酸和次氯酸,单质与水不能拆,弱电解质次氯酸不能拆,故离子反应方程式为:Cl2+H2O═H++Cl-+HClO,
故答案为:Cl2+H2O═H++Cl-+HClO.
(1)A、B、C、D分别为:氮、氧、硫、氯,元素符号分别为:N、O、S、Cl,故答案为:N、O、S、Cl;
(2)D为Cl,处于第三周期第VIIA族,故答案为:三;VIIA;
(3)氯气与水反应生成盐酸和次氯酸,单质与水不能拆,弱电解质次氯酸不能拆,故离子反应方程式为:Cl2+H2O═H++Cl-+HClO,
故答案为:Cl2+H2O═H++Cl-+HClO.
点评:本题主要考查原子结构与元素周期表,难度不大,推断元素是解题关键,注意离子反应方程式的书写.

练习册系列答案
相关题目
能证明胶体微粒比溶液中电解质微粒大的操作是( )
| A、丁达尔效应 | B、布朗运动 |
| C、渗析 | D、电泳现象 |
下列描述正确的是( )
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可通过溶液导电能力的大小判断强弱电解质 |
| D、在NaHSO4溶液中存在的离子有:Na+、H+、HSO4-、OH- |
下列关于离子反应的叙述中,错误的是( )
| A、溶液中发生的复分解反应肯定是离子反应 |
| B、离子反应并不一定要有水、有气体、有沉淀生成才能发生 |
| C、醋酸钠中滴入硫酸也能发生离子反应 |
| D、氯气和水的反应不属于离子反应 |
将某Mg-Al合金放入足量的盐酸中,生成H2 的体积在标况下是2240ml;同质量的Mg-Al合金放入足量的NaOH溶液中生成H2 的体积在标况下是2016ml,则Mg、Al的质量之比是( )
| A、1:1 | B、6:1 |
| C、1:6 | D、4:27 |
某条件下锌与稀硝酸反应时其物质的量之比为5:12,则此时硝酸的还原物是( )
| A、NO2 |
| B、NO |
| C、N2O |
| D、N2 |
两种气态烃的混合气共0.1mol,在空气中完全燃烧得到0.16molCO2和3.6g水,下列说法正确的是( )
| A、一定含甲烷,不含乙烷 |
| B、一定含乙烷,不含甲烷 |
| C、一定是甲烷和乙烯的混合物 |
| D、一定含甲烷,但不含乙烯 |