题目内容
13.硒(Se)位于周期表中第4周期、第ⅥA族,根据它在周期表中的位置推测,硒不可能具有的性质是( )| A. | H2Se的热稳定性比 H2S的稳定性强 | B. | SeO3的水化物是一种含氧酸 | ||
| C. | 硒元素有+6、+4、-2等常见化合价 | D. | Se的单质在常温下呈固态 |
分析 A.元素的非金属性越强,其氢化物的稳定性越强;
B.Se和S为同一主族元素,其单质和化合物具有相似的性质,SO3的水化物是一种含氧酸;
C.Se元素性质和S相似,其存在的化合价相似;
D.氧族元素中,随着原子序数增大其单质有气态变为固态.
解答 解:A.元素的非金属性越强,其氢化物的稳定性越强,非金属性S>Se,所以H2Se的热稳定性比 H2S的稳定性弱,故A错误;
B.Se和S为同一主族元素,其单质和化合物具有相似的性质,SO3的水化物硫酸是一种含氧酸,所以SeO3的水化物硒酸是一种含氧酸,故B正确;
C.Se元素性质和S相似,其存在的化合价相似,Se元素有+6、+4、-2等常见化合价,故C正确;
D.氧族元素中,随着原子序数增大其单质有气态变为固态,氧族元素中,氧气是气体,其它单质是固态,故D正确;
故选A.
点评 本题考查元素周期律,为高频考点,明确同一主族元素原子结构、元素性质是解本题关键,同一主族元素结构、性质相似,采用知识迁移方法分析解答.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
3.下列化合物的分子中,所有原子都处于同一平面的有( )
| A. | 乙烷 | B. | 甲苯 | C. | 乙苯 | D. | 四氯乙烯 |
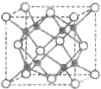
4.图为氯化钠的晶体结构模型,下列说法不正确的是( )


| A. | NaC1晶体中Na+与C1-的个数比为1:1 | |
| B. | 每个Na+周围距离最近的C1-数为6 | |
| C. | 和Na+距离相等且最近的C1-构成的多面体是正八面体 | |
| D. | 每个Na+周围距离最近的Na+数为8 |
1.下列物质中,既能与盐酸又能与氢氧化钠溶液反应,且均有气体生成的化合物是( )
| A. | Si | B. | NH4HCO3 | C. | Al | D. | Al2O3 |
8.下列物质由于发生反应,不能使溴水褪色,但能使酸性KMnO4溶液褪色的是( )
| A. | 异丁烷 | B. | 1-戊烯 | C. | 苯 | D. | 甲苯 |
18.常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A. | 提高溶液的温度 | B. | 加入适量的醋酸钠固体 | ||
| C. | 加入等体积0.2mol•L-1盐酸 | D. | 将溶液稀释到原体积的10倍 |

 元素X基态原子核外电子数为29,元素Y位于X的前一周期且最外层电子数为1,元素Z基态原子3p轨道上有4个电子,元素P原子最外层电子数是其内层电子数的3倍,元素Q基态原子2p半充满.请回答下列问题:
元素X基态原子核外电子数为29,元素Y位于X的前一周期且最外层电子数为1,元素Z基态原子3p轨道上有4个电子,元素P原子最外层电子数是其内层电子数的3倍,元素Q基态原子2p半充满.请回答下列问题: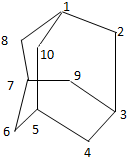 有的油田开采的石油中溶有一种碳氢化合物-金刚烷.
有的油田开采的石油中溶有一种碳氢化合物-金刚烷.