题目内容
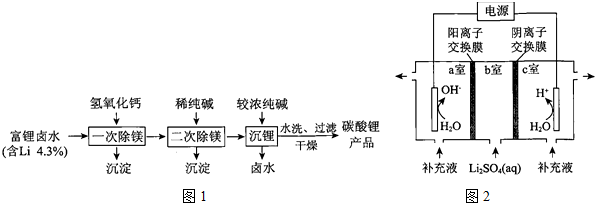
5.K3[Fe(C2O4)3]•3H2O[三草酸合铁(Ⅲ)酸钾晶体]是制备负载型活性铁催化剂的主要原料,也是一些有机反应很好的催化剂.如图1是在实验室中制备K3[Fe(C2O4)3]•3H2O的流程:回答下列问题:

(1)步骤Ⅰ中加入稀硫酸的目的是抑制Fe2+水解.
步骤Ⅱ中发生的主要反应为一可逆反应,其离子方程式为Fe2++H2C2O4?FeC2O4↓+2H+.
常温下,该反应的平衡常数K=0.56[已知常温下:Ka1(H2C2O4)=5.6×10-3、Ka2(H2C2O4)=2.1×10-5、Ksp(FeC2O4)=2.1×10-7].
(2)下列试剂均可将FeC2O4氧化为K3[Fe(C2O4)3],最适宜作为“试剂a”的是c(填序号)
a.氯水 b.酸性KMnO4溶液 c.H2O2溶液 d.稀硝酸
(3)使用托盘天平称量制得的K3[Fe(C2O4)3]•3H2O的质量.天平平衡时,右盘内砝码的总质量为20g,游码示数如图2所示,则制得晶体的质量为21.9g,该实验中K3[Fe(C2O4)3]•3H2O的产率为44.6%.(已知:K3[Fe(C2O4)3]•3H2O[的相对分子质量为491,FeSO4•7H2O的相对分子质量为278)
分析 制备K3[Fe(C2O4)3]•3H2O的流程:硫酸亚铁加入稀硫酸抑制Fe2+水解,硫酸亚铁与草酸反应生成草酸亚铁沉淀,用过氧化氢将草酸亚铁氧化为K3[Fe(C2O4)3],加入草酸溶液煮沸后,一定条件下结晶得到K3[Fe(C2O4)3]•3H2O晶体.
(1)亚铁离子在水溶液中水解,加入稀硫酸抑制水解;步骤Ⅱ中发生(NH4)2Fe(SO4)2•6H2O+H2C2O4═FeC2O4↓+(NH4)2SO4+H2SO4+6H2O,本质为亚铁离子和草酸生成草酸亚铁的沉淀,根据其离子反应方程式结合Ka1(H2C2O4)=5.6×10-3、Ka2(H2C2O4)=2.1×10-5、Ksp(FeC2O4)=2.1×10-7]书写该反应的平衡常数;
(2)双氧水为绿色氧化剂,反应后煮沸即可过量的双氧水;
(3)被测物体的质量等于砝码的总质量与游码所对刻度之和.根据铁原子守恒计算出理论K3[Fe(C2O4)3]•3H2O质量,产率=$\frac{实际产量}{理论产量}$×100%.
解答 解:(1)步骤Ⅰ中:亚铁离子在水溶液中水解:Fe2++2H2O?Fe(OH)2+2H+,溶解的过程中要加入几滴稀硫酸,目的是抑制Fe2+水解,步骤Ⅱ中发生(NH4)2Fe(SO4)2•6H2O+H2C2O4═FeC2O4↓+(NH4)2SO4+H2SO4+6H2O,本质为亚铁离子和草酸生成草酸亚铁的沉淀,所以离子反应为:Fe2++H2C2O4?FeC2O4↓+2H+,化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,常温下,该反应的平衡常数K=$\frac{{C}^{2}({H}^{+})}{C(F{e}^{2+})×C({H}_{2}{C}_{2}{O}_{4})}$=$\frac{{K}_{a1}×{K}_{a2}}{{K}_{sp}}$=$\frac{5.6×1{0}^{-3}×2.1×1{0}^{-5}}{2.1×1{0}^{-7}}$=0.56,
故答案为:抑制Fe2+水解;Fe2++H2C2O4?FeC2O4↓+2H+;0.56;
(2)将FeC2O4氧化为K3[Fe(C2O4)3],最适宜作为“试剂a”是H2O2溶液,反应为 2FeC2O4+H2O2+3K2C2O4+H2C2O4═2K3[Fe(C2O4)3]↓+2H2O,温度较高时,H2O2分解,反应后煮沸即可过量的双氧水,其它氧化剂引入杂质,
故答案为:C;
(3)在天平的标尺上,1g之间有10个小格,一个小格代表的质量是0.1g,即天平的分度值为0.1g;被测物体的质量为20g+1.9g=21.9g,27.6克FeSO4•7H2O,物质的量为$\frac{27.6g}{276g/mol}$=0.1mol,根据铁原子守恒,理论生成K3[Fe(C2O4)3]•3H2O的物质的量为0.1mol,质量为:0.1mol×491g/mol=49.1g,产率=$\frac{实际产量}{理论产量}$×100%=$\frac{21.9g}{49.1g}$×100%≈44.6%,
故答案为:21.9;44.6%.
点评 本题考查了物质制备实验过程分析判断,为高频考点,把握发生的化学反应及实验操作为解答的关键,侧重分析能力的考查,注意信息与所学知识的结合,题目难度中等.

| 元素 | 元素性质或原子结构信息 |
| A | A元素的一种核素无中子 |
| B | B原子的次外层电子数等于最外层电子数的一半 |
| W | W的单质常温下为双原子分子,其氢化物的水溶液呈碱性 |
| G | G原子M层上有6个电子 |
| E | E元素的最高正价是+7 |
(2)B元素的最高价氧化物对应的水化物属于共价化合物(填‘离子化合物’或‘共价化合物’);
(3)W元素的最高价氧化物对应水化物能与其氢化物发生化合反应,反应方程式为HNO3+NH3=NH4NO3.
(4)元素G与元素E相比,非金属性较强的是氯(填元素名称),下列表述能证明这一事实的是b(填序号).
a.常温下E单质和G单质的密度不同;
b.E的氢化物比G的氢化物稳定;
c.E的氢化物水溶液酸性比G的氢化物水溶液酸性强
d.一定条件下G和E的单质都能与氢氧化钠溶液反应.
| A. | M元素一定是第VA族元素 | |
| B. | M元素一定是第三周期元素 | |
| C. | M可形成与CH3CHO电子数相等的化合物 | |
| D. | M的单质在空气中加热时可能会生成红棕色气体 |
| A. | H2Se的热稳定性比 H2S的稳定性强 | B. | SeO3的水化物是一种含氧酸 | ||
| C. | 硒元素有+6、+4、-2等常见化合价 | D. | Se的单质在常温下呈固态 |
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$mol/(L•min) | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 三个容器中反应的平衡常数均为K=2 |
| A. | C2H5Br | B. | 氯水 | C. | 溴的CCl4溶液 | D. | KClO3溶液 |
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由Cl元素和S元素的最低化合价分别为-1和-2,推知元素的非金属性S>Cl |
 短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.
短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.