题目内容
18.市售盐酸试剂中溶质的质量分数为36.5%,密度为1.18g/ml,该盐酸的物质的量浓度是11.9mol/L.分析 根据c=$\frac{1000ρw}{M}$计算.
解答 解:c=$\frac{1000ρw}{M}$=$\frac{1000×1.19×36.5%}{36.5}$mol/L=11.9mol/L,
故答案为:11.9.
点评 本题考查物质的量浓度和质量分数之间的换算、浓溶液的稀释,题目难度不大,注意相关计算公式的运用.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
8.已知:a.C2H2(g)+H2(g)=C2H4(g)△H<0 b.2CH4(g)=C2H4(g)+2H2(g)△H>0
判断以下3个热化学方程式:①C(s)+2H2(g)=CH4(g)△H1
②C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g)△H2③C(s)+H2(g)=$\frac{1}{2}$C2H4(g)△H3
△H1、△H2、△H3由大到小的顺序是( )
判断以下3个热化学方程式:①C(s)+2H2(g)=CH4(g)△H1
②C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g)△H2③C(s)+H2(g)=$\frac{1}{2}$C2H4(g)△H3
△H1、△H2、△H3由大到小的顺序是( )
| A. | △H2>△H3>△H1 | B. | △H3>△H2>△H1 | C. | △H3>△H1>△H2 | D. | △H1>△H2>△H3 |
9.恒温时,在体积为V的密闭容器内,可逆反应:N2+3H2?2NH3 达平衡时,测得容器内气体的压强为p1.将容器的体积压缩 $\frac{V}{2}$至达到新的平衡时,气体的压强为 p2.则 p1 和 p2 的关系为( )
| A. | p2<p1 | B. | p1<p2<2p 1 | C. | p1>2p2 | D. | 2p1=p2 |
6.下列事实不能用有机物分子内基团间的相互影响解释的是( )
| A. | 甲苯能使酸性KMnO4溶液褪色,而苯和甲烷不能 | |
| B. | 苯酚能跟NaOH溶液反应而乙醇不能 | |
| C. | 乙烯能发生加成反应而乙烷不能 | |
| D. | 苯在50-60℃时发生硝化反应生成硝基苯,而甲苯在30℃时即可发生硝化反应生成三硝基甲苯 |
13.几种短周期元素的原子半径及主要化合价如表:
已知X是短周期中最活泼的金属,且与R同周期.下列叙述不正确的是( )
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6、-2 | +5、-3 | -2 | +3 |
| A. | 离子半径大小:R3+<X+<M2- | |
| B. | Y与M组成的化合物是光化学烟雾的原因之一 | |
| C. | 将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 | |
| D. | R的单质是铝热剂的成分之一 |
10.对下列物质的化学用语书写正确的是( )
| A. | 乙烯的结构简式为CH2CH2 | B. | 羟基的电子式: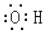 | ||
| C. | 苯酚的结构简式为C6H5OH | D. | 乙醇的分子式:CH3CH2OH |
7.下列物质属于纯净物的是( )
| A. | 冰水混合物 | B. | 无污染的空气 | C. | 氯水 | D. | 漂白粉 |