题目内容
10.对下列物质的化学用语书写正确的是( )| A. | 乙烯的结构简式为CH2CH2 | B. | 羟基的电子式: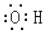 | ||
| C. | 苯酚的结构简式为C6H5OH | D. | 乙醇的分子式:CH3CH2OH |
分析 A、烯烃结构简式中的碳碳双键不能省略;
B、羟基中含一个未成对电子;
C、苯酚是一个-OH直接连在苯环上构成的;
D、表示元素组成的式子为分子式.
解答 解:A、烯烃结构简式中的碳碳双键不能省略,故乙烯的结构简式为CH2=CH2,故A错误;
B、羟基中含一个未成对电子,故-OH的电子式为 ,故B错误;
,故B错误;
C、苯酚是一个-OH直接连在苯环上构成的,故其结构简式为C6H5OH,故C正确;
D、表示元素组成的式子为分子式,故乙醇的分子式 为C2H6O,故D错误.
故选C.
点评 本题考查了常见的化学用语,难度不大,应注意区分分子式和结构简式的书写.

练习册系列答案
相关题目
1.在10L密闭容器中,1mol A和3mol B在一定条件下反应:A(g)+xB(g)?2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4mol C,则下列计算结果正确的是( )
| A. | 平衡时,物质的量之比n(A):n(B):n(C)=2:11:4 | |
| B. | x值等于3 | |
| C. | A的转化率为20% | |
| D. | B的平均反应速率为0.4 mol/(L•min) |
5.在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)?3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.
该反应的平衡常数表达式为K=$\frac{{c}^{3}(C)}{{c}^{2}(A)×c(B)}$.升高温度,平衡常数将减小(填“增大”“减小”或“不变”).
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 2 | 3 | 0 |
15.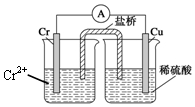 金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )
金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )
 金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )
金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )| A. | 盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液 | |
| B. | 理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池 | |
| C. | 此过程中H+得电子,发生氧化反应 | |
| D. | 电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中 |
2.实验室用H2SO4滴定氨水,选用的指示剂是( )
| A. | 甲基橙 | B. | 石蕊 | C. | 酚酞 | D. | 任选一种均可以 |
19.除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是( )
| A. | Al2O3(SiO2):NaOH溶液 | B. | CO2(SO2):饱和的Na2CO3溶液 | ||
| C. | NaHCO3溶液(Na2CO3溶液):Ca(OH)2溶液 | D. | FeCl2溶液(FeCl3):Fe粉 |