题目内容
6.为了除去粗盐中的Ca2+、Mg2+、SO42-,可将粗盐溶于水,然后进行 ①过滤②加适量的NaOH溶液③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液等五项操作.正确的操作顺序是( )| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ③⑤②④① |
分析 除去粗盐中的Ca2+、Mg2+、SO42-,加碳酸钠除去钙离子,加NaOH除去镁离子,加氯化钡除去硫酸根离子,且碳酸钠一定在氯化钡之后,以此来解答.
解答 解:除去粗盐中的Ca2+、Mg2+、SO42-,加碳酸钠除去钙离子,加NaOH除去镁离子,加氯化钡除去硫酸根离子,且碳酸钠一定在氯化钡之后,最后加盐酸蒸发,则正确的顺序为②⑤④①③或⑤②④①③,
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握粗盐提纯、实验技能为解本题关键,侧重分析与实验能力的考查,注意试剂的加入顺序及除杂原则,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
17.关于共价键,下列说法不正确的是( )
| A. | 按共用电子对是否偏移,可以把共价键划分为极性键和非极性键 | |
| B. | 按原子轨道的重叠方式,分为σ键和π 键 | |
| C. | 按共用电子对的提供方式,分为配位键和普通共价键 | |
| D. | 所有分子中都含有共价键 |
14.下列依据相关实验得出的结论正确的是( )
| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| B. | 将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质 | |
| C. | 在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3 | |
| D. | 加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在 |
1.在盛放浓硫酸的试剂瓶上应印有如图所示警示标记中的( )
| A. |  | B. |  | C. |  | D. | 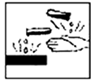 |
11.设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 1摩尔CH4所含质子数目为10NA | |
| C. | 0.2NA个硫酸分子与19.6g磷酸含有相同的氢原子数 | |
| D. | 18g NH4+所含中子数目为10 NA |
18.NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1molCl2溶于足量水中,转移的电子数为0.1NA | |
| B. | 100g98%的浓硫酸中,氧原子总数为4NA | |
| C. | 常温常压下,3g甲醛所含σ键数目为0.3NA | |
| D. | 1molFeCl3与沸水反应生成胶体后,含有的Fe(OH)3胶粒数目为NA |
15.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 50℃时,1LpH=1的H2SO4溶液含H+的数目为0.1NA | |
| B. | 1mol锌与浓硫酸完全反应生成SO2和H2的混合气体,气体的分子数小于NA | |
| C. | 100gCaCO3和KHCO3混合固体中的CO32-的数目为NA | |
| D. | 标准状况下,2.24L苯含有的原子数为1.2NA |
1.如图,下列各情况,在其中Fe片腐蚀由慢到快的顺序是( )

| A. | ⑤②①③④ | B. | ⑤①②④③ | C. | ④②①③⑤ | D. | ④③①②⑤ |

