题目内容
14.下列反应中,属于吸热反应的是( )| A. |  | B. |  | ||
| C. |  | D. |  |
分析 化学反应过程中一定伴随能量变化,反应可以是放热反应或吸热反应,反应物能量可以高于生成物反应放热,反应物能量低于生成物,反应吸热反应,据此分析解答.
解答 解:图中横坐标表示反应过程,纵坐标表示能量,B、D反应物的总能量低于生成物,高出的能量需放出,C反应物的总能量等于生成物,化学反应中反应物的能量与生成物的能量一定不同,所以不存在该反应,只有A,反应物能量低于生成物,需从外部吸收,属于吸热反应,
故选A.
点评 本题考查反应能量变化的分析判断,掌握基础、理解实质是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.能用H++OH-=H2O来表示的化学反应是( )
| A. | NaOH溶液与碳酸反应 | B. | Cu(OH)2与稀硝酸反应 | ||
| C. | Ba(OH)2溶液与稀硫酸反应 | D. | KOH溶液与稀盐酸反应 |
5.下列各组物质中,化学键类型完全相同的是( )
| A. | HI和NaI | B. | H2O2和CO2 | C. | Cl2和CCl4 | D. | MgCl2和NaBr |
2.下列说法不正确的是( )
| A. | 不能自发进行的氧化还原反应,通过电解的原理可以实现 | |
| B. | 电镀时保持电流恒定,升高温度不改变电解反应速率 | |
| C. | 电解精炼铜电解槽底部会形成含少量Ag、Fe、Pt等金属的阳极泥 | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 | |
| E. | MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液,若电解电路中通过2mol电子,MnO2的理论产量为1mol | |
| F. | 燃料电池是将燃料燃烧所放出的能量转化为化学能的装置 |
9.某硝酸盐R(NO3)2受热分解为RO、NO2、O2,在标准状况下,将生成的气体充满一烧瓶,并将烧瓶倒置于水中,当烧瓶中液面不再上升时烧瓶内溶液浓度是( )
| A. | $\frac{4}{5}$mol•L-1 | B. | $\frac{1}{14}$mol•L-1 | C. | $\frac{1}{22.4}$mol•L-1 | D. | $\frac{1}{28}$mol•L-1 |
19.下列性质能代表卤素通性的是( )
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(浓)═Na2SO4+2HX |
6.己知反应:①PbO2+4HCI═PbCl2+C12↑+2H20,②Cu+2Fe3+═Cu2++2Fe2+,③Cl2+2Fe2+═2Cl-+2Fe3+.则有关物质(离子)的氧化性由强到弱的顺序为( )
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
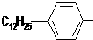
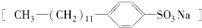 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: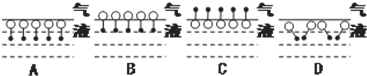
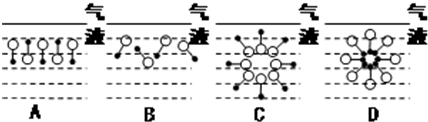
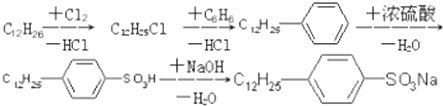
 .
.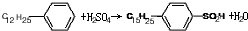 ,反应类型为取代反应.
,反应类型为取代反应.