题目内容
下列有关化学用语的表述正确的是( )
A、CO2的电子式: | ||
B、甲烷分子的比例模型: | ||
C、原子核内有20个中子的氯原子:
| ||
| D、乙烯的结构简式:CH2CH2 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.二氧化碳为共价化合物,分子中含有两个碳氧双键,碳原子和氧原子最外层达到8电子稳定结构;
B.甲烷为正四面体结构,碳原子比较大于氢原子;
C.元素符号的左上角表示的是质量数、左下角表示质子数;
D.结构简式中必须标出有机物的官能团,乙烯分子中含有碳碳双键.
B.甲烷为正四面体结构,碳原子比较大于氢原子;
C.元素符号的左上角表示的是质量数、左下角表示质子数;
D.结构简式中必须标出有机物的官能团,乙烯分子中含有碳碳双键.
解答:
解:A.二氧化碳分子中存在两个碳氧双键,C、O原子的最外层都达到8电子稳定结构,二氧化碳正确的电子式为: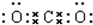 ,故A错误;
,故A错误;
B.比例模型能够体现出分子中各原子的相对体积大小,甲烷分子中碳原子半径大于氢原子,甲烷的比例模型为; ,故B正确;
,故B正确;
C.氯元素的质子数为17,原子核内有20个中子的氯原子,其质量数为37,该氯原子可以表示为:1737Cl,故C错误;
D.乙烯分子中含有碳碳双键,其结构简式中应该标出官能团,乙烯正确的结构简式为:CH2=CH2,故D错误;
故选B.
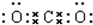 ,故A错误;
,故A错误;B.比例模型能够体现出分子中各原子的相对体积大小,甲烷分子中碳原子半径大于氢原子,甲烷的比例模型为;
 ,故B正确;
,故B正确;C.氯元素的质子数为17,原子核内有20个中子的氯原子,其质量数为37,该氯原子可以表示为:1737Cl,故C错误;
D.乙烯分子中含有碳碳双键,其结构简式中应该标出官能团,乙烯正确的结构简式为:CH2=CH2,故D错误;
故选B.
点评:本题考查了电子式、比例模型、结构简式、元素符号的表示方法判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确比例模型与球棍模型、共价化合物与离子化合物的电子式的区别.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列叙述正确的是( )
| A、一定温度和压强下,各气态物质体积大小主要由构成气体的分子数决定 |
| B、摩尔质量就是该物质的相对分子质量或相对原子质量 |
| C、单位物质的量的物质所占的体积就是气体摩尔体积 |
| D、40g NaOH溶解在1L水中.形成溶液溶质的物质的量浓度为1mol/L |
L-香芹醇是一种重要的香料原料,其结构简式如图所示,下列有关说法不正确的是( )


| A、分子式为C10H16O |
| B、能使酸性高锰酸钾溶液橙色 |
| C、能与金属钠反应 |
| D、能发生加成反应和水解反应 |
根据表中信息判断,下列选项正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-… | Cl2、Mn2+… |
| A、第①组反应的其余产物为H2O |
| B、第②组反应中Cl2与FeBr2的物质的量之比大于或等于1:2 |
| C、第③组反应中生成1mol Cl2,转移电子5mol |
| D、氧化性由强到弱顺序为MnO4->Cl2>Br2>Fe3+ |
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是( )
| A、0.1mol?L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO32-) |
| B、0.1mol?L-1 Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
| C、0.1mol?L-1(NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| D、0.1mol?L-1 NH4Cl溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
宇航员在升空、返回或遇到紧急情况时,必须穿上10公斤重的舱内航天服,神舟系列宇航员所穿舱内航天服是我国科学家近年来研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅(SiC)、陶瓷和碳纤维复合而成,下列相关叙述错误是( )
| A、它耐高温 |
| B、它没有固定熔点 |
| C、它是由多种材料组成的复合材料 |
| D、它是一种新型有机材料 |
