题目内容
8. A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )
A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )| A. | 4.32 g | B. | 2.16 g | C. | 1.08 g | D. | 0.54 g |
分析 根据图知,Cu、Ag是阴极,C是阳极,B装置和C装置并联,BC装置和A装置串联,当通电一段时间后,如若A中铜电极的质量增加1.28g时,A中析出金属是Cu,n(Cu)=$\frac{1.28g}{64g/mol}$=0.02mol,B中银电极上析出Ag,因为BC装置并联,所以析出Cu时有一半的电子通过B中银电极,根据转移电子守恒计算n(Ag),再根据m(Ag)=nM计算.
解答 解:根据图知,Cu、Ag是阴极,C是阳极,B装置和C装置并联,BC装置和A装置串联,当通电一段时间后,如若A中铜电极的质量增加1.28g时,A中析出金属是Cu,n(Cu)=$\frac{1.28g}{64g/mol}$=0.02mol,B中银电极上析出Ag,因为BC装置并联,所以析出Cu时有一半的电子通过B中银电极,根据转移电子守恒得n(Ag)=$\frac{0.02mol×2×\frac{1}{2}}{1}$=0.02mol,m(Ag)=nM=0.02mol×108g/mol=2.16g,故选B.
点评 本题考查电解原理,为高频考点,明确电路的串并联及通过B中银电极的电子数是解本题关键,注意:通过Cu的电子有一半电子通过B装置中的Ag,为易错点.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
20.下列说法正确的是( )
| A. | 呈酸性的雨水就是酸雨 | B. | “雷雨肥庄稼”符合科学道理 | ||
| C. | 光化学烟雾是由二氧化硫引起的 | D. | 臭氧层破坏与氮氧化物无关 |
1.X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X、Z同主族,Y、Q同主族,X是周期表中所有元素原子半径最小的,Y是所有元素中非金属性最强的元素.W元素所处周期的序数等于其族序数.下列说法正确的是( )
| A. | 离子半径:Q>W>Z>Y | |
| B. | 元素Y、Q的气态氢化物稳定性:Q>Y | |
| C. | 元素Z、W、Q的最高价氧化物对应水化物相互间能发生反应 | |
| D. | Y与X、Y与Z形成的化合物化学键类型相同. |
13.下列叙述错误的是( )
| A. | 金属钠在自然界中能以游离态存在 | |
| B. | 金属钠着火时,用细沙覆盖灭火 | |
| C. | 易燃试剂与强氧化性试剂分开放置并远离火源 | |
| D. | 钠在空气中燃烧生成过氧化钠 |
20.下列关于CO2和SO2气体的说法不正确的是( )
| A. | 与足量的澄清石灰水反应的现象不同 | |
| B. | 通入BaCl 2溶液时现象相同 | |
| C. | 通入Ba(NO3)₂溶液时现象相同 | |
| D. | 通入石蕊溶液时现象相同 |
17. 纽扣电池可用于计算器、电子表等的电源.有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O═2Ag+ZnO.关于该电池的叙述不正确的是( )
纽扣电池可用于计算器、电子表等的电源.有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O═2Ag+ZnO.关于该电池的叙述不正确的是( )
 纽扣电池可用于计算器、电子表等的电源.有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O═2Ag+ZnO.关于该电池的叙述不正确的是( )
纽扣电池可用于计算器、电子表等的电源.有一种纽扣电池,其电极分别为Zn和Ag2O,以KOH溶液为电解质溶液,电池的总反应为Zn+Ag2O═2Ag+ZnO.关于该电池的叙述不正确的是( )| A. | 作用时电子由Zn极经外电路流向Ag2O极,Zn是负极 | |
| B. | 使用时电子由Ag2O极经外电路流向Zn极,Ag2O是负极 | |
| C. | 正极的电极反应为Ag2O+2e-+H2O═2Ag+2OH- | |
| D. | Zn极发生氧化反应,Ag2O极发生还原反应 |
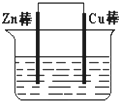 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置.试回答下列问题: