题目内容
20.下列说法正确的是( )| A. | 呈酸性的雨水就是酸雨 | B. | “雷雨肥庄稼”符合科学道理 | ||
| C. | 光化学烟雾是由二氧化硫引起的 | D. | 臭氧层破坏与氮氧化物无关 |
分析 A.酸雨是PH小于5.6的雨水;
B.根据雷电的固氮作用和具有使植物生长茂盛、叶色浓绿功能的肥料种类为氮肥判断;
C.氮的氧化物是引起光化学烟雾的主要原因;
D.臭氧空洞的形成与氟氯烃或氮氧化物有关.
解答 解:A.酸雨是PH小于5.6的雨水,所以呈酸性的雨水不一定是酸雨,故A错误;
B.空气中的氮气和氧气能在放电的条件下反应生成一氧化氮,一氧化氮易氧化为二氧化氮,再与水反应最终生成硝酸混于雨水中,在土壤中又会进一步形成硝酸盐,能使植物生长茂盛、叶色浓绿的肥料是氮肥,故B正确;
C.大气中碳氢化合物和氮氧化合物在阳光的作用下起化学反应所产生的化学污染物,故C错误;
D.臭氧空洞的形成与氟氯烃或氮氧化物在大气中泄漏与臭氧(O3)发生一系列连锁反应有关,故D错误;
故选B.
点评 本题考查了酸雨、“雷雨肥庄稼”、光化学污染、臭氧层破坏等问题,题目难度不大,注意酸雨成分以及光化学烟雾等热点环境问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 电池中的重金属等污染土壤,可以回收再利用以减少污染、保护资源 | |
| C. | 人们日常生活中用到各种化学品,应尽量减少甚至不使用 | |
| D. | 城市机动车成为PM2.5(直径≤2.5微米的颗粒物,也称为可入肺颗粒物,有毒、有害)主要源头,必须加以控制 |
8.下列关于元素周期表的说法中正确的是( )
| A. | 过渡元素全部是金属元素 | |
| B. | 同周期第ⅡA族与第ⅢA族元素的原子序数差值一定是1 | |
| C. | 催化剂一般在金属与非金属的分界线处寻找 | |
| D. | 同一主族元素的原子序数的差不可能为10 |
15.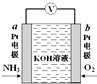 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )| A. | 溶液中OH-向电极a移动 | |
| B. | 负极的电极反应式为:2NH3-6e-+6OH-═N2↑+6H2O | |
| C. | O2在电极b上发生还原反应 | |
| D. | 反应消耗的NH3与O2的物质的量之比为4:5 |
5.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色溶液中:K+、Na+、MnO4-、SO42- | |
| B. | 碱性溶液中:Na+、S2-、SO32-、AlO2- | |
| C. | 酸性溶液中:Na+、Fe2+、SO42-、NO3- | |
| D. | 加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
12.如表实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向氯水中加入硝酸银溶液,有白色沉淀产生 | 氯水中已无Cl2 |
| B | 将SO2通入酸性高锰酸钾溶液,溶液紫色褪去 | SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入少量铁粉,没有红色固体析出 | 氧化性:Fe3+>Cu2+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
8. A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )
A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )
 A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )
A、B、C三个电解槽,如图所示A中为CuCl2溶液,B、C中均为AgNO3溶液(其中电极的大小、形状、间距均相同),B、C中浓度和体积相同,当通电一段时间后,如若A中铜电极的质量增加1.28g时,B中电极上银增加的质量为( )| A. | 4.32 g | B. | 2.16 g | C. | 1.08 g | D. | 0.54 g |