题目内容
2.用NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 0.5 mol O3与11.2 L O2所含的分子数一定相等 | |
| B. | 标准状况下,11.2 L由N2与CO组成的混合气体含有的原子数目为NA | |
| C. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压下,22.4 L的NO2和CO2混合气体含有2NA个氧原子 |
分析 A.氧气状况未知,Vm不确定;
B.依据n=$\frac{V}{Vm}$计算混合气体的物质的量,结合氮气、一氧化碳都是双原子分子解答;
C.气体摩尔体积使用对象为气体;
D.常温常压Vm≠22.4L/mol.
解答 解:A.氧气状况未知,Vm不确定,无法计算氧气的物质的量和分子数,故A错误;
B.氮气、一氧化碳都是双原子分子,标准状况下,11.2 L由N2与CO组成的混合气体物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,所以含有原子数目为0.5mol×2×NA=NA,故B正确;
C.标况下四氯化碳为液体,不能使用气体摩尔体积,故C错误;
D.常温常压Vm≠22.4L/mol,Vm未知,无法计算混合气体的物质的量和氧原子个数,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意气体摩尔体积使用条件和对象.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
12.下列叙述正确的是( )
| A. | 95℃纯水的 pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液,稀释至 10 倍后 pH=4 | |
| C. | pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH>7 | |
| D. | pH 均为3的醋酸和盐酸分别与足量Zn反应,醋酸产生的H2多 |
13.下列溶液中能用来区别SO2和CO2气体的是( )
①石灰水
②H2S溶液
③酸性KMnO4
④氯水
⑤品红溶液
⑥紫色石蕊试液.
①石灰水
②H2S溶液
③酸性KMnO4
④氯水
⑤品红溶液
⑥紫色石蕊试液.
| A. | ①②③⑤ | B. | ①⑥ | C. | ① | D. | ②③④⑤ |
10.金属钠应保存在( )
| A. | 煤油中 | B. | 水中 | C. | 棕色瓶中 | D. | 四氯化碳中 |
17.下列有关说法正确的是( )
| A. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| B. | 甲烷是天然气的主要成分,能发生取代反应,但不能发生氧化反应 | |
| C. | 只用水无法鉴别苯、乙酸和四氯化碳 | |
| D. | 植物油不能用于萃取溴水中的溴 |
7.下列化学用语正确的是( )
| A. | 乙酸的结构简式 C2H4O2 | B. | 氯化钠的电子式: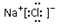 | ||
| C. | 硫原子的原子结构示意图: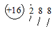 | D. | 水的电离方程式 2H2O═H3O++OH- |
14.下列有关物质的性质与用途具有对应关系的是( )
| A. | 明矾溶于水能形成氢氧化铝胶体,可用于自来水的杀菌消毒 | |
| B. | 氧化镁熔点高,可用于耐高温材料 | |
| C. | 碳酸钠具有碱性,可用于胃酸中和剂 | |
| D. | 铝能置换出氧化铁中的铁,可用于钢铁工业中大量冶炼铁 |
11.下列说法中正确的是( )
| A. | 向海水中加入净水剂明矾可以使海水淡化 | |
| B. | 开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 | |
| C. | 海水淡化的方法主要有电渗析法、蒸馏法、离子交换法等 | |
| D. | 海洋植物具有富集碘的能力,因此从海产品中提取碘是工业上获取碘的重要途径,工业从海带中提取碘经历的步骤有:浸泡-过滤-氧化-萃取-粗碘提纯 |
12.某实验小组同学模拟工业制碘的方法,探究ClO3-和I-的反应规律.实验操作及现象如下:
(1)取实验2后的溶液,进行如图1实验:
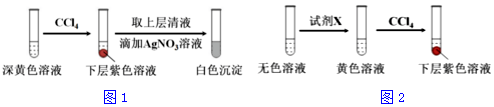
经检验,上述白色沉淀是AgCl.写出加入0.20mLNaClO3后,溶液中ClO3-和I-发生反应的离子方程式:
ClO3-+6I-+6H+=Cl-+3I2+3H2O.
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-.
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2.
进行实验:
①取少量实验4中的无色溶液进行如图2实验,进一步佐证其中含有IO3-.其中试剂X可以是c(填字母序号).
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化.进行以上对比实验的目的是进一步佐证4中生成了Cl2.
获得结论:NaClO3溶液用量增加导致溶液褪色原因是2ClO3-+I2=Cl2↑+2IO3-(用离子方程式表示).
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
①对比实验4和5,可以获得的结论是ClO3-和I-的反应规律与H+(或H2SO4)的用量有关
②用离子方程式解释实验6的现象:6ClO3-+5I-+6H+=3Cl2↑+5IO3-+3H2O.
| 实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
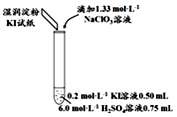 | 1 | 0.05mL | 浅黄色 | 无色 |
| 2 | 0.20mL | 深黄色 | 无色 | |
| 3 | 0.25mL | 浅黄色 | 蓝色 | |
| 4 | 0.30mL | 无色 | 蓝色 |

经检验,上述白色沉淀是AgCl.写出加入0.20mLNaClO3后,溶液中ClO3-和I-发生反应的离子方程式:
ClO3-+6I-+6H+=Cl-+3I2+3H2O.
(2)查阅资料:一定条件下,I-和I2都可以被氧化成IO3-.
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是过量的NaClO3溶液与(1)中的反应产物继续反应,同时生成Cl2.
进行实验:
①取少量实验4中的无色溶液进行如图2实验,进一步佐证其中含有IO3-.其中试剂X可以是c(填字母序号).
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
②有同学提出,仅通过湿润淀粉KI试纸变蓝的现象不能说明生成Cl2,便补充了如下实验:将实验4中的湿润淀粉KI试纸替换为湿润的淀粉试纸,再滴加0.30mL1.33mol•L-1NaClO3溶液后,发现湿润的淀粉试纸没有明显变化.进行以上对比实验的目的是进一步佐证4中生成了Cl2.
获得结论:NaClO3溶液用量增加导致溶液褪色原因是2ClO3-+I2=Cl2↑+2IO3-(用离子方程式表示).
(3)小组同学继续实验,通过改变实验4中硫酸溶液的用量,获得如表实验结果:
| 编号 | 6.0mol•L-1 H2SO4 溶液用量 | 试管中溶液颜色 | 淀粉KI试纸颜色 |
| 5 | 0.25mL | 浅黄色 | 无色 |
| 6 | 0.85mL | 无色 | 蓝色 |
②用离子方程式解释实验6的现象:6ClO3-+5I-+6H+=3Cl2↑+5IO3-+3H2O.