题目内容
8.工业上,可用硫酸铈溶液吸收尾气中NO,其化学方程式如下:2NO+3H2O+4Ce(SO4)2=2Ce2(SO4)3+HNO3+HNO2+2H2SO4下列说法正确的是( )| A. | 在该反应中氧化剂与还原剂的物质的量之比为1:2 | |
| B. | 在该反应中,氧化产物有两种,还原产物有一种 | |
| C. | 若不考虑溶液体积变化,吸收尾气后,溶液的pH将增大 | |
| D. | 在该反应中,每消耗22.4LNO必转移2 mol电子 |
分析 2NO+3H2O+4Ce(SO4)2=2Ce2(SO4)3+HNO3+HNO2+2H2SO4中,1N元素由+2升高到+5价,1N元素由+2升高到+3价,Ce元素由+4降低到+3价,据此分析解答.
解答 解:A.1N元素由+2升高到+5价,1N元素由+2升高到+3价,则NO是还原剂,Ce元素由+4降低到+3价,则硫酸铈是氧化剂,氧化剂、还原剂的物质的量之比为2:1,故A错误;
B.硫酸铈是氧化剂,生成Ce2(SO4)3为还原产物,NO是还原剂,生成HNO2、HNO3是氧化产物,所以在该反应中,氧化产物有两种,还原产物有一种,故B正确;
C.反应后生成硫酸,则溶液的酸性增强,pH减小,故C错误;
D.没有限制“标准状况”,不能计算转移电子数目,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.取浓度相同的NaOH和HCl溶液,以3:2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为( )
| A. | 0.01 mol/L | B. | 0.07 mol/L | C. | 0.05 mol/L | D. | 0.50 mol/L |
16.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,4g H2含有的分子数为 2NA | |
| B. | 18g H2O在标准状况下的体积是22.4L | |
| C. | 2.3g金属钠变为钠离子时失去的电子数为NA | |
| D. | 通常状况下,NA个CO2分子占有的体积为22.4L |
3.下列叙述正确的是( )
| A. | 1molH2O的质量为18g/mol | B. | CH4的摩尔质量为16g | ||
| C. | 3.01×1023个SO2分子的质量为32g | D. | 0.05mol SO2的体积是1.12L |
13.高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O,下列说法正确的是( )
| A. | ClO-做还原剂 | B. | Fe(OH)3在反应中被还原 | ||
| C. | 高铁酸钾中铁的化合价为+7 | D. | 制备1molK2FeO4时转移3 mol 电子 |
20.下列仪器可以直接加热的是( )
| A. | 烧杯 | B. | 烧瓶 | C. | 锥形瓶 | D. | 试管 |
17.在相同温度下,0.01mol•L-1NaOH溶液和0.01mol•L-1的盐酸相比,下列说法正确的是( )
| A. | 两溶液中由水电离出c(H+)都是1.0×10-12 mol•L-1 | |
| B. | NaOH溶液和盐酸中由水电离出c(OH-)分别为1.0×10-2mol•L-1、1.0×10-12 mol•L-1 | |
| C. | 两溶液中由水电离出的c(H+)相等 | |
| D. | 两者都促进了水的电离 |
18.下列有关说法错误的是( )
| A. | 为保护海轮的船壳,常在船壳上镶入锌块 | |
| B. | 纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应 | |
| C. | 已知工业合成氨△H<O,达平衡后,升高温度,正反应速率减少、逆反应速率增大,平衡向逆反应方向移动 | |
| D. | NH3(g)+HCl(g)═NH4Cl(s)较低温下能自发进行,说明该反应的△H<O |
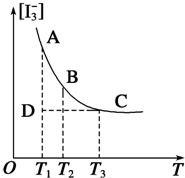 实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq).上述平衡体系中,I3-的物质的量浓度[I3-]与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).
实验室中配制碘水,往往是将I2溶于KI溶液中,这样就可以得到浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq).上述平衡体系中,I3-的物质的量浓度[I3-]与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).