题目内容
2.下列离子最容易结合H+的是( )| A. | OH- | B. | CH3COO- | C. | CH3CH2O- | D. | ClO- |
分析 电解质的电离程度越大,对应的阴离子越易结合氢离子,如能形成非电解质,则结合氢离子的程度最大,以此解答该题.
解答 解:酸性CH3COOH>HClO>H2O,则结合氢离子的难易程度为OH->ClO->CH3COO-,而CH3CH2OH为非电解质,则CH3CH2O-更易结合H+,
故选C.
点评 本题考查弱电解质的电离以及强弱电解质的比较,侧重考查学生的分析能力,注意把握比较的角度以及相关知识的把握,难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案
相关题目
12.某有机物的分子式为C4H6O2,下列说法不正确的是( )
| A. | 可能含有一个酯基和一个碳碳双键 | B. | 可能含有一个醛基和一个羰基 | ||
| C. | 可能含有一个环和一个酯基 | D. | 可能含有一个醛基和一个碳碳叁键 |
13. 某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
 某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl溶液是电解质 | |
| B. | 电解质在电流的作用下才发生电离 | |
| C. | NaCl溶液中的水电离出大量的离子 | |
| D. | NaCl在水溶液中存在自由移动的离子是溶液能导电的原因 |
10. 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )| 甲 | 乙 | 丙 | 戊 | |
| A | Cu | FeCl3溶液 | CuCl2溶液 | Fe |
| B | H2O | Fe | H2 | O2 |
| C | CH3CH2OH | O2 | CH3CHO | H2 |
| D | SiO2 | Na2CO3 | Si | O2 |
| A. | A | B. | B | C. | C | D. | D |
17.下列电离方程式中,书写不正确的是( )
| A. | Ba(OH)2═Ba2++2 OH- | B. | H3PO4 3?H++PO43- | ||
| C. | HI=H++I- | D. | NH3•H2O?NH4++OH- |
7.下列说法正确的是( )
| A. | 氢键、分子间作用力、离子键、共价键都是微粒间的作用力,其中氢键、离子键和共价键是化学键 | |
| B. | 石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 | |
| C. | 下列物质的熔沸点由大到小排列:晶体硅>碳化硅>金刚石 | |
| D. | 黄色晶体碳化铝,熔点2200℃,熔融态不导电,是原子晶体 |
14.在酸性溶液中能大量共存而且溶液为无色透明的是( )
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、SO42-、Ba2+ | ||
| C. | K+、MnO4-、NH4+、Cl- | D. | Ca2+、K+、HCO3-、NO3- |
11.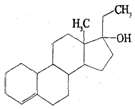 为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述错误的是( )
为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述错误的是( )
 为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述错误的是( )
为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如图所示.下列叙述错误的是( )| A. | 分子式为C20H30O | |
| B. | 能使溴的四氯化碳溶液褪色 | |
| C. | 能发生加成、取代、氧化反应 | |
| D. | 在浓硫酸作用下,分子内脱去一个水分子,产物有两种 |
12.下列化学反应属于氧化还原反应的是( )
| A. | CaCO3+2HCl=CaCl2+CO2↑+H2O | B. | CuO+2HCl=CuCl2+H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | NaOH+HCl=NaCl+H2O |