题目内容
怎样用化学方法除去下列物质中混有的少量杂质(用有关反应的离子方程式).
(1)铜粉中混有铁粉
(2)Na2CO3溶液中混有NaHCO3
(3)FeCl2溶液中混有CuCl2 .
(1)铜粉中混有铁粉
(2)Na2CO3溶液中混有NaHCO3
(3)FeCl2溶液中混有CuCl2
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:除杂的原则是:不增:不增加新的杂质;不减:不减少被提纯物质;易分离:杂质与被提纯物质容易分离.
(1)铜粉中混有铁粉利用金属活泼性加入盐酸除去铁;
(2)Na2CO3溶液中混有NaHCO3 加入少量的氢氧化钠;
(3)FeCl2溶液中混有CuCl2加人过量的铁粉.
(1)铜粉中混有铁粉利用金属活泼性加入盐酸除去铁;
(2)Na2CO3溶液中混有NaHCO3 加入少量的氢氧化钠;
(3)FeCl2溶液中混有CuCl2加人过量的铁粉.
解答:
解:(1)铜粉中混有铁粉利用金属活泼性加入盐酸除去铁,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(2)Na2CO3溶液中混有NaHCO3 加入少量的氢氧化钠,反应的离子方程式为HCO3-+OH-=H2O+CO32-,故答案为:HCO3-+OH-=H2O+CO32-;
(3)FeCl2溶液中混有CuCl2加人过量的铁粉,反应的离子方程式为Fe+Cu2+=Cu+Fe2+,故答案为:Fe+Cu2+=Cu+Fe2+.
(2)Na2CO3溶液中混有NaHCO3 加入少量的氢氧化钠,反应的离子方程式为HCO3-+OH-=H2O+CO32-,故答案为:HCO3-+OH-=H2O+CO32-;
(3)FeCl2溶液中混有CuCl2加人过量的铁粉,反应的离子方程式为Fe+Cu2+=Cu+Fe2+,故答案为:Fe+Cu2+=Cu+Fe2+.
点评:本题考查物质的提纯和离子反应方程式,题目简单,解题时应注意选择合适的试剂,保证不增加新的杂质,不减少被提纯的物质,杂质和被提纯的物质容易分离,书写离子方程式注意离子的拆和留.

练习册系列答案
相关题目
绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.下列反应类型从理论上看原子利用率可达到100%的是( )
| A、加成反应 | B、分解反应 |
| C、酯化反应 | D、取代反应 |
下列各组中的离子,能在酸性溶液中大量共存的是( )
| A、Ba2+、Na+、SO42-、OH- |
| B、SO42-、Na+、H+、NO3- |
| C、H+、K+、Cl-、SO42- |
| D、Na+、K+、CO32-、NO3- |
某学生欲完成Cu+2Ag+=2Ag++Cu2+反应,设计了下列四个实验,可行的是( )
A、 稀盐酸 |
B、 CuSO4溶液 |
C、 AgNO3 |
D、 CuSO4溶液 |
蒸干灼烧下列物质的水溶液,能得到该物质的是( )
| A、NaHCO3 |
| B、Al(NO3)3 |
| C、Fe2(SO4)3 |
| D、(NH4)2CO3 |
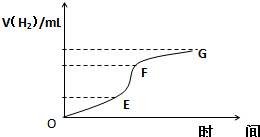 ( I)用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答:
( I)用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答: