题目内容
按要求回答下列问题
(1)用电子式表示H2S的形成过程 .
(2)用电子式表示MgCl2的形成过程 .
(3)试比较CH4与SO2在水中的溶解度大小并说明理由 .
(1)用电子式表示H2S的形成过程
(2)用电子式表示MgCl2的形成过程
(3)试比较CH4与SO2在水中的溶解度大小并说明理由
考点:用电子式表示简单的离子化合物和共价化合物的形成
专题:化学用语专题
分析:(1)硫化氢为共价化合物,根据共价化合物的电子式表示方法写出硫化氢的形成过程;
(2)MgCl2为离子化合物,根据离子化合物的电子式表示方法写出硫化钠的形成过程;
(3)水是极性分子,根据相似相溶原理判断.
(2)MgCl2为离子化合物,根据离子化合物的电子式表示方法写出硫化钠的形成过程;
(3)水是极性分子,根据相似相溶原理判断.
解答:
解:(1)硫化氢为共价化合物,分子中存在两个H-S键,用电子式表示其形成过程为: ,
,
故答案为: .;
.;
(2)MgCl2为离子化合物,用电子式表示氯化镁的形成过程为: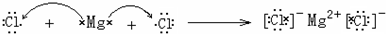 ;
;
故答案为: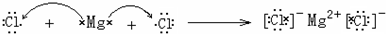 ;
;
(3)SO2中S原子的价层电子对为3,VSEPR模型为平面三角形,S原子1对孤对电子对,分子为V形,结构不对称,属于极性分子,CH4是非极性分子,水是极性分子,根据相似相溶原理,SO2在水中的溶解度比CH4的大,且SO2还能与H2O发生反应生成亚硫酸,也增大了SO2的溶解度;
故答案为:在水中的溶解度:SO2>CH4,因为H2O、SO2均是极性分子,CH4是非极性分子,根据相似相溶原理,SO2的溶解度大于CH4的溶解度,且SO2还能与H2O发生反应生成亚硫酸,也增大了SO2的溶解度.
 ,
,故答案为:
 .;
.;(2)MgCl2为离子化合物,用电子式表示氯化镁的形成过程为:
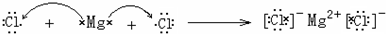 ;
;故答案为:
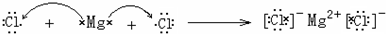 ;
;(3)SO2中S原子的价层电子对为3,VSEPR模型为平面三角形,S原子1对孤对电子对,分子为V形,结构不对称,属于极性分子,CH4是非极性分子,水是极性分子,根据相似相溶原理,SO2在水中的溶解度比CH4的大,且SO2还能与H2O发生反应生成亚硫酸,也增大了SO2的溶解度;
故答案为:在水中的溶解度:SO2>CH4,因为H2O、SO2均是极性分子,CH4是非极性分子,根据相似相溶原理,SO2的溶解度大于CH4的溶解度,且SO2还能与H2O发生反应生成亚硫酸,也增大了SO2的溶解度.
点评:本题考查了用电子式表示化合物形成过程、相似相溶原理,题目难度中等,要求学生熟练掌握电子式的概念及表示方法,能够用电子式正确表示离子化合物、共价化合物的形成过程.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
一种新型绿色电池-燃料电池,是把H2、CO、CH4气体和空气不断输入直接氧化,使化学能转变为电能,它被称为21世纪的绿色发电站,这三种气体可以作为燃料电池所需燃料的理由是( )
| A、都是无毒无害气体 |
| B、在自然界都大量存在 |
| C、都可以燃烧并放出大量的热 |
| D、燃烧产物均为CO2和H2O |
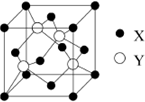 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.