题目内容
“物质的组成和结构决定物质性质,物质的性质决定了物质的用途”.请分析:
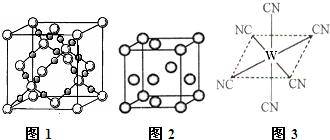
(1)金刚石很硬,而石墨却很软.原因是 .
(2)氢氧化钠和氢氧化钡溶液都能使无色酚酞试液变红.原因是 .
(3)CO具有可燃性,可以做燃料;CO具有还原性,可以用来 .(答一点即可)
(1)金刚石很硬,而石墨却很软.原因是
(2)氢氧化钠和氢氧化钡溶液都能使无色酚酞试液变红.原因是
(3)CO具有可燃性,可以做燃料;CO具有还原性,可以用来
考点:物质的组成、结构和性质的关系
专题:元素及其化合物,化学应用
分析:(1)主要从碳原子排列的方式不同分析解答;
(2)酚酞遇到碱变红色;
(3)依据一氧化碳的性质推断其用途.
(2)酚酞遇到碱变红色;
(3)依据一氧化碳的性质推断其用途.
解答:
解:(1)金刚石和石墨互为同素异形体,都是碳的单质,但是因为碳原子排列方式不同,所以导致二者硬度不同,
故答案为:碳原子排列方式不同;
(2)氢氧化钠和氢氧化钡都是碱,在水中能够电离产生氢氧根离子,使溶液显碱性,酚酞与碱变红色,
故答案为:两种溶液都能解离出氢氧根离子;
(3)一氧化碳具有可燃性所以可做燃料;一氧化碳具有还原性能将金属氧化物还原出来,故可冶炼金属,故答案:冶炼金属.
故答案为:碳原子排列方式不同;
(2)氢氧化钠和氢氧化钡都是碱,在水中能够电离产生氢氧根离子,使溶液显碱性,酚酞与碱变红色,
故答案为:两种溶液都能解离出氢氧根离子;
(3)一氧化碳具有可燃性所以可做燃料;一氧化碳具有还原性能将金属氧化物还原出来,故可冶炼金属,故答案:冶炼金属.
点评:本题考查了物质的结构和性质及用途,题目难度不大,注意同素异形体物理性质差别较大,化学性质相似.

练习册系列答案
相关题目
已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=+489.0kJ?mol-1①CO(g)+
O2(g)═CO2(g)△H=-283.0kJ?mol-1②C(石墨)+O2(g)═CO2(g)△H=-393.5kJ?mol-1③则4Fe(s)+3O2(g)═2Fe2O3(s)的△H为( )
| 1 |
| 2 |
| A、+1164.1kJ?mol-1 |
| B、-1641.0kJ?mol-1 |
| C、-259.7kJ?mol-1 |
| D、-519.4kJ?mol-1 |
下列有关实验的叙述,正确的是( )
| A、乙烷和氯气光照下制取纯净的氯乙烷 |
| B、用分液漏斗分离环己烷和水的混合液体 |
| C、用浓氨水洗涤做过银镜反应的试管 |
| D、在苯和溴水的混合物中加入铁粉制取溴苯 |
下列说法不正确的是( )
| A、比较多电子原子中电子能量大小的依据是电子离原子核的远近 |
| B、各能级最多容纳的电子数是该能级原子轨道数的二倍,其理论依据是构造原理 |
| C、电子排布在同一能级时,总是自由配对,优先占据同一轨道,且自旋方向相反 |
| D、钠的焰色与原子核外电子发生跃迁有关 |
设NA为阿伏加德罗常数,下面叙述正确的是( )
| A、标准状况下,11.2L SO3所含分子数为0.5 NA |
| B、1L 1mol/L的氯化钠溶液中,所含离子数为NA |
| C、64g二氧化硫含有原子数为3NA |
| D、在反应中,1mol镁转化为Mg2+后失去的电子数为NA |