题目内容
11.下列实验方案能达到预期目的是( )①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO42-
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼矾,铝作还原剂.
| A. | ②④⑤ | B. | ①②⑤ | C. | ①②④ | D. | ②③④ |
分析 ①FeCl3与Fe粉发生氧化还原反应;
②氢氧化钠溶液可腐蚀玻璃瓶;
③可能含有SO32-;
④淀粉溶液具有胶体的性质;
⑤铝比钒活泼,可用于冶炼金属.
解答 解:①FeCl3与Fe粉发生氧化还原反应,不能加入铁,否则变质,故错误;
②玻璃中含有二氧化硅,氢氧化钠溶液可腐蚀玻璃瓶,保存时应用橡胶塞,故正确;
③可能含有SO32-,应先加入盐酸,如无现象再加入氯化钡检验,故错误;
④淀粉溶液具有胶体的性质,具有丁达尔效应,故正确;
⑤铝比钒活泼,可用铝热法冶炼金属,故正确.
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的性质实验,把握化学反应原理、物质的性质为解答的关键,注意方案的评价性、操作性分析,题目难度不大.

练习册系列答案
相关题目
2.某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示.下列有关说法不正确的是( )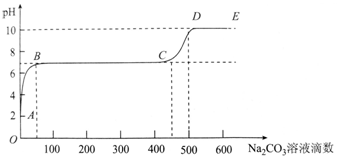

| A. | 开始时溶液pH=2是因为残留液中还有盐酸剩余 | |
| B. | BC段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加 | |
| C. | AB发生的反应为:Ca2++CO32-═CaCO3↓ | |
| D. | 滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+) |
19.-种制取粗碘的工艺流程如图所示,下列有关说法错误的是( )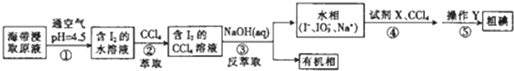

| A. | 步骤②中的萃取过程为物理变化 | |
| B. | 步骤③发生的反应中I2是氧化剂,NaOH是还原剂 | |
| C. | 步骤④所加的试剂X可能是稀硫酸 | |
| D. | 步骤⑤涉及的主要操作Y为分液和蒸馏 |
6.32.5gZn投入到VmL浓硫酸中,共热,恰好完全反应,则可以确定的数据是( )
| A. | 所得气体在标准状况下的体积 | B. | 所得气体的质量 | ||
| C. | 所得溶液的浓度 | D. | 原硫酸的浓度 |
16.禁止运动员使用兴奋剂是2012绿色奥运的重要举措之一,下图是兴奋剂利尿酸的结构 .关于它的说法正确的是( )
.关于它的说法正确的是( )
 .关于它的说法正确的是( )
.关于它的说法正确的是( )| A. | 利尿酸的化学式为:C13H14O4Cl2 | |
| B. | 利尿酸最多可与4 molH2发生反应 | |
| C. | 利尿酸可使溴的四氯化碳溶液褪色 | |
| D. | 利尿酸在一定条件下能发生消去反应 |
3.有关于化学实验的操作或者说法中,正确的是( )
| A. | 用加热法测定胆矾晶体中结晶水含量时,若在空气中冷却会使结果偏低 | |
| B. | 配制氯化铁溶液时,先将氯化铁溶于较浓盐酸,再用蒸馏水稀释并加入少量铁粉 | |
| C. | 将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,即可提纯甲烷 | |
| D. | 将蔗糖和稀硫酸混合加热后,再加入银氨溶液并水浴加热,以检验还原性糖 |
1.下列说法不正确的是( )
| A. | 氢氧化铁胶体可用于净水 | |
| B. | 镁合金可用于制造导弹、飞机的部件 | |
| C. | 石灰石-石膏法可用于燃煤的脱硫 | |
| D. | 焦炭在炼铁高炉中用于直接还原铁矿石 |