题目内容
1.下列说法不正确的是( )| A. | 氢氧化铁胶体可用于净水 | |
| B. | 镁合金可用于制造导弹、飞机的部件 | |
| C. | 石灰石-石膏法可用于燃煤的脱硫 | |
| D. | 焦炭在炼铁高炉中用于直接还原铁矿石 |
分析 A.氢氧化铁胶体具有较大表面积,有吸附性;
B.镁合金密度小,硬度大;
C.依据方程式:SO2+Ca(OH)2=CaSO3+H2O;2CaSO3+O2=2CaSO4解答;
D.炼铁过程中,焦炭燃烧生成二氧化碳,二氧化碳在高温条件下被焦炭还原成一氧化碳,一氧化碳和铁矿石反应生成铁和二氧化碳.
解答 解:A.氢氧化铁胶体具有较大表面积,有吸附性,能够吸附水中杂质,可以做净水剂,故A正确;
B.镁合金密度小,硬度大,适合制造导弹、飞机的部件,故B正确;
C.石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2═CaSO3+H2O,然后再将产物氧化制成石膏,2CaSO3+O2=2CaSO4,故C正确;
D.焦炭在炼铁高炉中先和空气中的氧气反应生成二氧化碳,二氧化碳再被焦炭还原成一氧化碳,一氧化碳和铁矿石反应生成铁和二氧化碳,不是用焦炭还原铁矿石,故D错误;
故选:D.
点评 本题考查了元素化合物知识及高炉炼铁原理,明确氢氧化铁胶体、合金的性质,熟悉燃煤的脱硫方法和原理、高炉炼铁原理是解题关键,题目难度中等,注意对相关知识的积累.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
11.下列实验方案能达到预期目的是( )
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO42-
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼矾,铝作还原剂.
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO42-
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼矾,铝作还原剂.
| A. | ②④⑤ | B. | ①②⑤ | C. | ①②④ | D. | ②③④ |
12.下列说法不正确的是( )
| A. | 氯气可用于自来水的消毒 | B. | 二氧化硅是半导体材料 | ||
| C. | 氢氧化铁胶体能用于净水 | D. | 二氧化硫可用于漂白纸浆 |
9.认真审题,完成下列实验探究.
(1)探究潮湿氯气与碳酸钠反应的产物
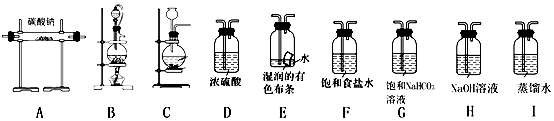
①选择必要的仪器,按BFAH顺序连接好装置(填装置序号).
②写出在该实验情境下,制备氯气的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③将A中充分反应后的固体物质分成两等份分装于两支试管中.
向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,由此现象推断固体产物中含有NaHCO3;向另一支试管中滴加过量的稀HNO3,再滴加AgNO3溶液,溶液变浑浊,由此现象推断固体产物中含有NaCl;
又已知A中反应还生成黄红色的Cl2O气体,请结合上述成分分析过程,写出潮湿的Cl2和Na2CO3的化学方程式2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O.
(2)二氧化碳与过氧化钠反应探究.
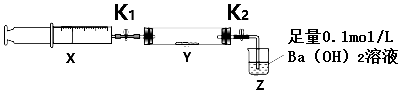
将一定量(过量)二氧化碳充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按如图示装置进行实验.
(1)探究潮湿氯气与碳酸钠反应的产物

①选择必要的仪器,按BFAH顺序连接好装置(填装置序号).
②写出在该实验情境下,制备氯气的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
③将A中充分反应后的固体物质分成两等份分装于两支试管中.
向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,由此现象推断固体产物中含有NaHCO3;向另一支试管中滴加过量的稀HNO3,再滴加AgNO3溶液,溶液变浑浊,由此现象推断固体产物中含有NaCl;
又已知A中反应还生成黄红色的Cl2O气体,请结合上述成分分析过程,写出潮湿的Cl2和Na2CO3的化学方程式2Cl2+2Na2CO3+H2O=2NaCl+2NaHCO3+Cl2O.
(2)二氧化碳与过氧化钠反应探究.
将一定量(过量)二氧化碳充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按如图示装置进行实验.

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | ①淡黄色固体变为白色粉末 | ②反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2 |
| 将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | ③Z中液体出现倒吸 | ④不用解释 |
16.下列各组物质的熔点均与所含化学键的键能有关的是( )
| A. | CaO 与CO2 | B. | NaCl与HCI | C. | SiC 与SiO2 | D. | CCl4与I2 |
6.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1molOH-与1mol-OH所含质子数均为9NA | |
| B. | 0.1mol/L的CuCl2溶液中含Cl-的数目为0.2 NA | |
| C. | 标准状况下,11.2LCCl4中含C-C键的数目为2NA | |
| D. | 10 mL 2mol/LH2O2完全分解,转移的电子数为0.2 NA |
13.美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如图所示),下列有关说法正确的是( )
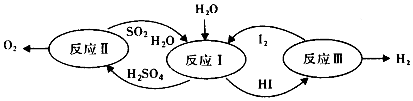

| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1mol O2的同时产生1molH2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
10.下列物质在水溶液中的电离方程式书写正确的是( )
| A. | KClO3═K++3O2-+Cl5+ | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2SO4═H++SO42- | D. | Al2(SO4)3═2Al3++3SO42- |