题目内容
11.下列关于物质“反应程度”的说法正确的是( )| A. | 一定条件下,2 mol SO2与足量O2反应,可制备2 mol SO3 | |
| B. | 一定条件下,1 mol N2与3 mol H2反应,可制备1.0 mol NH3 | |
| C. | 10 mL 18.0 mol/L 的H2SO4与足量铜加热反应,可制备0.09 mol SO2 | |
| D. | 含4 mol HCl的浓盐酸与足量MnO2加热反应,可制备1 mol Cl2 |
分析 A、SO2和氧气之间的反应是可逆的,不能将物质完全转化;
B、1mol N2与3mol H2反应的产物氨气的量会小于2mol;
C、金属铜可以和浓硫酸之间反应,但是和稀硫酸之间不反应;
D、二氧化锰只能和浓盐酸反应,和稀盐酸之间不会发生反应.
解答 解:A、一定条件下,2molSO2与足量O2反应得到SO3的量会小于2mol,故A错误;
B、一定条件下,1mol N2与3mol H2反应不能进行彻底,产生氨气的量会小于2mol,可以获得1.0mol NH3,故B正确;
C、10mL 18.0mol/L H2SO4与足量铜加热反应,随着反应的进行,硫酸变稀,Cu和稀硫酸之间不反应,可制备SO2的物质的量小于0.09mol,故C错误;
D、含4mol HCl的浓盐酸与足量的MnO2加热反应,随着反应的进行,盐酸变稀,二氧化锰只能和浓盐酸反应,和稀盐酸之间不会发生反应,反应可制备Cl2的物质的量小于1mol,故D错误;
故选B.
点评 本题涉及物质的性质以及化学反应的可逆性等方面的知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
相关题目
13.除去下列物质中所含的少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 选项 | 混合物 | 试剂 | 分离方法 |
| A | 苯(苯酚) | NaOH溶液 | 分液 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙酸(乙醇) | 金属钠 | 蒸馏 |
| D | C17H35COONa(甘油) | NaCl | 结晶 |
| A. | A | B. | B | C. | C | D. | D |
2.下列关于有机物的说法正确的是( )
| A. | 乙烯能使酸性KMnO4溶液和溴水褪色,二者反应原理相同 | |
| B. | 交警用酸性重铬酸钾溶液检查司机是否饮酒过量时乙醇发生取代反应 | |
| C. | 乙酸的分子式为C2H4O2,属于弱酸 | |
| D. | 苯分子中没有碳碳双键,因此苯不能发生加成反应 |
19. CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
 CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A. | 反应开始2分钟内平均反应速率最大 | |
| B. | 反应4分钟后平均反应速率最小 | |
| C. | 反应开始4分钟内温度对反应速率的影响比浓度大 | |
| D. | 反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小 |
6.某有机化合物M的结构简式为 ,有关该化合物的叙述正确的是( )
,有关该化合物的叙述正确的是( )
 ,有关该化合物的叙述正确的是( )
,有关该化合物的叙述正确的是( )| A. | 该有机物属于芳香烃 | |
| B. | 该有机物不易溶于水 | |
| C. | 该有机物不能被酸性高锰酸钾氧化 | |
| D. | 该有机物只能发生加成反应和酯化反应 |
16.某有机物的结构简式为 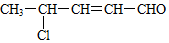 ,该有机物不可能发生的化学反应是( )
,该有机物不可能发生的化学反应是( )
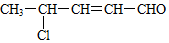 ,该有机物不可能发生的化学反应是( )
,该有机物不可能发生的化学反应是( )| A. | 加成反应 | B. | 酯化反应 | C. | 氧化反应 | D. | 水解反应 |
3.我国古代曾用火法炼铜:Cu2S+O2$\stackrel{高温}{→}$2Cu+SO2,下列说法正确的是( )
| A. | 铜元素发生了氧化反应 | B. | 反应中只有O2得电子 | ||
| C. | 32gO2参与反应,转移电子4mol | D. | Cu2S既被氧化又被还原 |
14.下列各组离子中,可以大量共存的是( )
| A. | Ag+、NO3-、Cl- | B. | OH-、Cl-、NH4+ | C. | Ba2+、Cl-、SO42- | D. | Mg2+、Cl-、NO3- |