题目内容
13.除去下列物质中所含的少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )| 选项 | 混合物 | 试剂 | 分离方法 |
| A | 苯(苯酚) | NaOH溶液 | 分液 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙酸(乙醇) | 金属钠 | 蒸馏 |
| D | C17H35COONa(甘油) | NaCl | 结晶 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯酚与NaOH溶液反应后,与苯分层;
B.乙烯与氢气发生加成反应,乙烷中可能混有氢气;
C.二者均与Na反应;
D.NaCl可降低C17H35COONa的溶解度.
解答 解:A.苯酚与NaOH溶液反应后,与苯分层,然后分液可分离,故A正确;
B.乙烯与氢气发生加成反应,乙烷中可能混有氢气,应选溴水、洗气分离,故B错误;
C.二者均与Na反应,不能除杂,故C错误;
D.NaCl可降低C17H35COONa的溶解度,发生盐析,析出晶体后过滤可分离,故D错误;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、混合物分离提纯方法为解答的关键,侧重分析与实验能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
9.葡萄糖在人体中进行无氧呼吸产生乳酸,乳酸的结构简式为 .下列有关乳酸的说法不正确的是( )
.下列有关乳酸的说法不正确的是( )
 .下列有关乳酸的说法不正确的是( )
.下列有关乳酸的说法不正确的是( )| A. | 乳酸能发生催化氧化、取代反应 | |
| B. | 乳酸和葡萄糖所含官能团相同 | |
| C. | 乳酸能和碳酸氢钠、钠反应放出气体 | |
| D. | 乳酸和HO-CH2-CH2-COOH互为同分异构体 |
4.下列图示与对应的叙述错误的是( )
| A. | 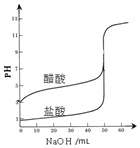 表示分别用NaOH溶液滴定等浓度等体积的盐酸和醋酸溶液反应变化曲线,指示剂都可用酚酞 | |
| B. |  表示分别用等浓度AgNO3溶液滴定等浓度等体积的NaCl、NaBr及NaI溶液反应变化曲线,c为I- | |
| C. | 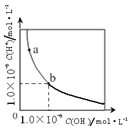 表示一定温度下,水溶液中H+和OH-的浓度变化曲线,b→a可能是加CuCl2溶液导致的 | |
| D. | 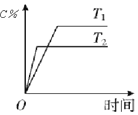 表示其他条件不变时,可逆反应A(g)+3B(g)?2C(g)△H<0,C的物质的量分数与温度的关系 |
1.下列反应的离子方程式书写正确的是( )
| A. | 惰性电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2+═4Na++2Cu(OH)2↓+O2↑ | |
| C. | 向NaClO和NaCl混合溶液中滴少量FeSO4溶液:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀物质的量最大:Al3++2SO42-+2Ba2++4OH-═[Al(OH)4]-+2BaSO4↓ |
8.下列说法正确的是( )
| A. | 实验室保存氯化铁溶液时常加入一根铁钉 | |
| B. | 工业上可用电解熔融的氯化铝制备金属铝 | |
| C. | 盐酸溶液和硫酸铁溶液中水的电离程度均增大 | |
| D. | 当甲烷-氧气-碱性(KOH溶液)燃料电池工作时,通入甲烷一极的电极反应式是:CH4+10OH--8e-═CO32-+7H2O |
18.不能用带橡胶塞的玻璃试剂瓶存放的药品是( )
①浓硝酸 ②稀氢氧化钠溶液 ③液溴 ④纯碱溶液 ⑤氢氟酸.
①浓硝酸 ②稀氢氧化钠溶液 ③液溴 ④纯碱溶液 ⑤氢氟酸.
| A. | ①③⑤ | B. | ②④ | C. | ①③ | D. | ①②③④⑤ |
5.下列物质在水溶液中的电离方程式正确的是( )
| A. | HCl═H++Cl- | B. | H2O═H++OH- | ||
| C. | Na2CO3?2Na++CO32- | D. | NH3•H2O═NH4++OH- |
10.可以用分液漏斗分离的一组液体混合物是( )
| A. | 苯和溴苯 | B. | 溴和四氯化碳 | C. | 苯和汽油 | D. | 水和溴苯 |
11.下列关于物质“反应程度”的说法正确的是( )
| A. | 一定条件下,2 mol SO2与足量O2反应,可制备2 mol SO3 | |
| B. | 一定条件下,1 mol N2与3 mol H2反应,可制备1.0 mol NH3 | |
| C. | 10 mL 18.0 mol/L 的H2SO4与足量铜加热反应,可制备0.09 mol SO2 | |
| D. | 含4 mol HCl的浓盐酸与足量MnO2加热反应,可制备1 mol Cl2 |