题目内容
2.下列关于有机物的说法正确的是( )| A. | 乙烯能使酸性KMnO4溶液和溴水褪色,二者反应原理相同 | |
| B. | 交警用酸性重铬酸钾溶液检查司机是否饮酒过量时乙醇发生取代反应 | |
| C. | 乙酸的分子式为C2H4O2,属于弱酸 | |
| D. | 苯分子中没有碳碳双键,因此苯不能发生加成反应 |
分析 A.乙烯含碳碳双键,与溴水发生加成反应、与高锰酸钾发生氧化反应;
B.乙醇含-OH,能被重铬酸钾氧化;
C.乙酸的分子式为C2H4O2,在水中不能完全电离;
D.苯无双键,为不饱和烃,可与氢气发生加成反应.
解答 解:A.乙烯含碳碳双键,与溴水发生加成反应、与高锰酸钾发生氧化反应,褪色的原理不同,故A错误;
B.乙醇含-OH,能被重铬酸钾氧化,则用酸性重铬酸钾溶液检查司机是否饮酒过量时乙醇发生氧化反应,故B错误;
C.乙酸的分子式为C2H4O2,在水中不能完全电离,为弱酸,故C正确;
D.苯无双键,为不饱和烃,可与氢气发生加成反应生成环己烷,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
4.下列图示与对应的叙述错误的是( )
| A. | 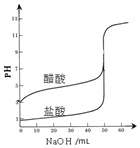 表示分别用NaOH溶液滴定等浓度等体积的盐酸和醋酸溶液反应变化曲线,指示剂都可用酚酞 | |
| B. |  表示分别用等浓度AgNO3溶液滴定等浓度等体积的NaCl、NaBr及NaI溶液反应变化曲线,c为I- | |
| C. | 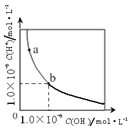 表示一定温度下,水溶液中H+和OH-的浓度变化曲线,b→a可能是加CuCl2溶液导致的 | |
| D. | 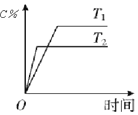 表示其他条件不变时,可逆反应A(g)+3B(g)?2C(g)△H<0,C的物质的量分数与温度的关系 |
5.下列物质在水溶液中的电离方程式正确的是( )
| A. | HCl═H++Cl- | B. | H2O═H++OH- | ||
| C. | Na2CO3?2Na++CO32- | D. | NH3•H2O═NH4++OH- |
10.可以用分液漏斗分离的一组液体混合物是( )
| A. | 苯和溴苯 | B. | 溴和四氯化碳 | C. | 苯和汽油 | D. | 水和溴苯 |
17.向含有CaCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
| A. | c(CO32-) | B. | c(Ca2+) | C. | c(H+) | D. | Ksp(CaCO3) |
7.一定条件下,在一体积不变的密闭容器中发生反应:N2(g)+3H2(g)?2NH3(g),能说明该反应达到化学平衡状态的是( )
| A. | N2、H2、NH3的浓度相等 | |
| B. | 容器内压强不再变化 | |
| C. | 单位时间内消耗a mol N2,同时生成2a mol NH3 | |
| D. | 容器内混合气体密度不再变化 |
14.NH3是一种重要的化工原料,在生产、生活中用途广泛.

(1)已知:
注:拆开气态物质中1mol某种共价键需要吸收的能量,就是该共价键的键能.
N2 (g)+3H2 (g)?2NH3 (g)△H=-92kJ•mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2+3H2?2NH3,测得各组分浓度随时间变化如图1所示.
①表示c(N2)的曲线是曲线A(填“曲线A”、“曲线B”或“曲线C”).
②0~t0时用H2表示反应速率v(H2)$\frac{0.6}{{t}_{0}}$mol•L-1•min-1.
③下列能说明该反应达到平衡的是a、d
a.混合气体的压强不再变化
b.2c(H2)=3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:
①电极b名称是正极.
②电解质溶液中OH-离子向电极a移动(填“电极a”或“电极b”).
③电极a的电极反应式为2NH3+6OH--6e-=N2+6H2O.
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4).该反应的化学反应方程式是2NH3+NaClO=N2H4+NaCl+H2O.

(1)已知:
| 共价键 | 键能/kJ•mol-1 |
| H-H | 436 |
N≡N | 946 |
| N-H | 391 |
N2 (g)+3H2 (g)?2NH3 (g)△H=-92kJ•mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2+3H2?2NH3,测得各组分浓度随时间变化如图1所示.
①表示c(N2)的曲线是曲线A(填“曲线A”、“曲线B”或“曲线C”).
②0~t0时用H2表示反应速率v(H2)$\frac{0.6}{{t}_{0}}$mol•L-1•min-1.
③下列能说明该反应达到平衡的是a、d
a.混合气体的压强不再变化
b.2c(H2)=3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:
①电极b名称是正极.
②电解质溶液中OH-离子向电极a移动(填“电极a”或“电极b”).
③电极a的电极反应式为2NH3+6OH--6e-=N2+6H2O.
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4).该反应的化学反应方程式是2NH3+NaClO=N2H4+NaCl+H2O.
11.下列关于物质“反应程度”的说法正确的是( )
| A. | 一定条件下,2 mol SO2与足量O2反应,可制备2 mol SO3 | |
| B. | 一定条件下,1 mol N2与3 mol H2反应,可制备1.0 mol NH3 | |
| C. | 10 mL 18.0 mol/L 的H2SO4与足量铜加热反应,可制备0.09 mol SO2 | |
| D. | 含4 mol HCl的浓盐酸与足量MnO2加热反应,可制备1 mol Cl2 |
12.亚硝酸钠(NaNO2)俗称“工业盐”,其外观与食盐相似,有咸味,有毒,可用作食品防腐剂和肉类食品的发色剂.已知亚硝酸钠能与氢碘酸(HI,具有强酸性)发生如下反应:4HI+2NaNO2═2NaI+I2+2NO↑+2H2O.下列说法错误的是( )
| A. | 人误食亚硝酸钠中毒时,不可以服用氢碘酸解毒 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 向反应所得的混合溶液中加入稀硫酸和亚硝酸钠,I-不可能转化为I2 | |
| D. | 当有2molHI被氧化时,转移电子数是2NA(设NA为阿伏加德罗常数的值) |