题目内容
14.以下各分子中,所有原子都满足最外层为8电子结构的是( )| A. | CO2 | B. | BF3 | C. | PCl5 | D. | H3O+ |
分析 对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,据此判断.
解答 解:A、CO2中,C原子的族序数+成键数=4+4=8,所以满足所有原子最外层为8电子结构,故A正确;
B、BF3中B元素化合价为+3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构;F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故B错误;
C、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故C错误;
D、H3O+中H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,故D错误.
故选A.
点评 本题考查原子核外电子排布和化学键,注意原子的最外层电子数及判断ABn型分子的一般规律来解答,题目难度中等.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
4.下列电离方程式书写正确的是( )
| A. | H2SO4→2H++SO42 | B. | Ba(OH)2→Ba2++(OH)2 | ||
| C. | FeCl3→Fe2++3Cl- | D. | NaHCO3→Na++H++CO32- |
5.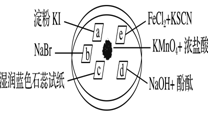 如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是( )
 如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O对实验现象的“解释或结论”正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | e处变红色 | 还原性:Fe2+>Cl- |
| D | d处立即褪色 | 氯气与水生成了漂白性物质 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关化学用语表示正确的是( )
| A. | NF3的电子式: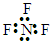 | B. | F-的结构示意图: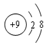 | ||
| C. | 中子数为18的硫原子:${\;}_{16}^{18}$S | D. | 乙酸甲酯的结构简式:HCOOCH2CH3 |
6.下列除去杂质的方法正确的是( )
| 物质(括号内为杂质) | 试剂 | |
| A | CO2(SO2) | Na2CO3溶液 |
| B | FeCl3溶液(CuCl2) | Fe |
| C | Fe2O3(Al2O3) | NaOH溶液 |
| D | Na2SO4溶液(Na2CO3) | 盐酸 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验装置、操作能达到实验目的是( )
| A. | 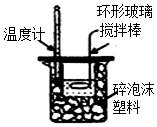 测定中和热 | B. | 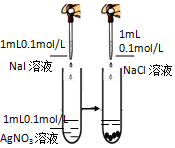 沉淀转化 | ||
| C. | 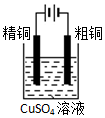 粗铜的电解精炼 | D. | 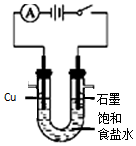 电解食盐水 |
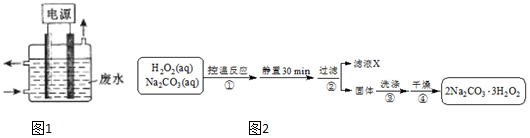
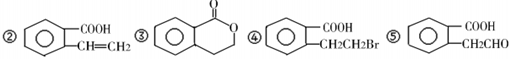
 ) 可以通过不同的反应得到②~⑤四种物质.
) 可以通过不同的反应得到②~⑤四种物质.