题目内容
设计一个原电池来实现反应:2Fe3++Fe=3Fe2+,下列各选项中,电极和电解质溶液选择正确的是( )
| 选项 | 负极材料 | 正极材料 | 电解质溶液 |
| A. | Cu | Fe | FeCl3 |
| B. | Zn | Fe | FeCl2 |
| C. | Fe | 石墨 | Fe2(SO4)3 |
| D. | Fe | Ag | Fe(NO3)2 |
| A、A | B、B | C、C | D、D |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据反应“2Fe3++Fe=3Fe2+”可知,反应中铁被氧化,应为原电池负极,因失电子而被氧化;正极应为活泼性比铁弱的金属或导电的非金属材料,Fe3+在正极得到电子而被还原,电解质溶液为含Fe3+的盐,以此解答.
解答:
解:A.Cu为负极,发生2Fe3++Cu=2Fe2++Cu2+,故A错误;
B.锌的活泼性大于铁,锌作负极,铁作正极,所以不能实现该反应的原电池,故B错误;
C.铁的活泼性大于C,铁作负极,C作正极,电解质溶液为Fe2(SO4)3溶液,所以是能实现该反应的原电池,故C正确;
D.铁的活泼性大于银,铁作负极,银作正极,但电解质溶液为Fe(NO3)2溶液,所以是不能实现该反应的原电池,故D错误.
故选C.
B.锌的活泼性大于铁,锌作负极,铁作正极,所以不能实现该反应的原电池,故B错误;
C.铁的活泼性大于C,铁作负极,C作正极,电解质溶液为Fe2(SO4)3溶液,所以是能实现该反应的原电池,故C正确;
D.铁的活泼性大于银,铁作负极,银作正极,但电解质溶液为Fe(NO3)2溶液,所以是不能实现该反应的原电池,故D错误.
故选C.
点评:本题考查原电池的设计及原电池的工作原理,题目难度不大,注意从氧化还原反应的角度确定原电池的电极材料及电解质溶液.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
升高温度,下列数据不一定增大的是( )
| A、电离平衡常数Ka |
| B、水解平衡常数Kb |
| C、化学平衡常数K |
| D、水的离子积常数Kw |
下列关于金属钠的叙述中正确的是( )
| A、钠可以保存在煤油或四氯化碳中 |
| B、钠长久露置在空气中最终生成NaHCO3 |
| C、钠在空气中燃烧,火焰黄色,生成淡黄色的Na2O2 |
| D、钠与水反应的实验现象可以说明钠硬度小、熔点低、密度小于水 |
下列各组离子能大量共存于同一溶液中的是( )
| A、Fe2+ H+ NO3- SO42- |
| B、Fe3+ NH4+ Cl- I- |
| C、Cu2+ Mg2+ NO3- Cl- |
| D、Al3+ Na+ SO42- OH- |
下列叙述正确的是( )
| A、液氨可用作致冷剂 |
| B、向Fe( OH ) 3 胶体中滴入过量的NaHSO4溶液,能使胶体发生凝聚而沉淀 |
| C、熔融状态下能够导电的化合物中一定存在离子键 |
| D、28g 乙烯和氮气的混合气体中含有NA个原子(戈代表阿伏加德罗常数的值) |
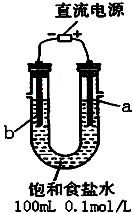 某化学研究小组用如图装置模拟步骤Ⅰ电解食盐水(用铁和石墨做电极材料).
某化学研究小组用如图装置模拟步骤Ⅰ电解食盐水(用铁和石墨做电极材料).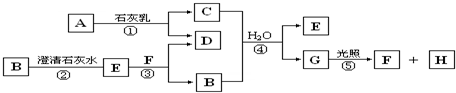
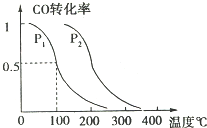 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.