题目内容
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | ||||
B、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
考点:离子方程式的书写
专题:
分析:A.漂白粉溶液在空气中失效,反应生成碳酸钙和HClO;
B.电荷、原子个数均不守恒;
C.碳酸氢钠与盐酸反应生成氯化钠、二氧化碳和水;
D.碱性环境下不能生成氢离子,不符合反应的客观事实.
B.电荷、原子个数均不守恒;
C.碳酸氢钠与盐酸反应生成氯化钠、二氧化碳和水;
D.碱性环境下不能生成氢离子,不符合反应的客观事实.
解答:
解:A.漂白粉溶液在空气中失效的离子反应为Ca2++2ClO-+CO2+H2O=2HClO+CaCO3↓,故A错误;
B.用浓盐酸与MnO2反应制取少量氯气,离子方程式:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故B错误;
C.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+=CO2↑+H2O,故C正确;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,离子方程式:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,故D错误;
故选:C.
B.用浓盐酸与MnO2反应制取少量氯气,离子方程式:MnO2+4H++2Cl-
| ||
C.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+=CO2↑+H2O,故C正确;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,离子方程式:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,题目难度不大,解题时注意化学式的拆分、反应是否遵循客观事实,选项AD为易错选项.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列说法错误的是( )
| A、二氧化硅是光导纤维的主要原料 |
| B、硅是信息技术的关键材料 |
| C、陶瓷餐具所用材料为硅酸盐 |
| D、水晶镜片所用原料为硅酸盐 |
测知由Fe2(SO4)3和FeSO4组成混合物中含硫a%,则其含铁量应为( )
| A、(100-4a)% |
| B、(100-2a)% |
| C、(100-a)% |
| D、(100-3a)% |
下列反应的离子方程式中,书写正确的是( )
| A、金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| B、将铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ |
| D、实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-═CO2↑+H2O |
下列电子式中正确的是:( )
A、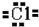 |
B、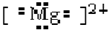 |
C、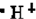 |
D、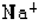 |
常温下某气态烃与氧气混合充入一容器中,点火爆炸后又恢复到原来温度,此时容器内压强为原来的一半,再经NaOH溶液处理,容器内几乎成为真空,则此烃分子式为( )
| A、C2H2 |
| B、C2H6 |
| C、C3H6 |
| D、C3H8 |