题目内容
下列电子式中正确的是:( )
A、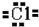 |
B、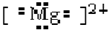 |
C、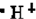 |
D、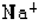 |
考点:电子式
专题:
分析:A.氯原子最外层7个电子;
B.阳离子的电子式与离子符号相同;
C.阳离子的电子式与离子符号相同;
D.阳离子的电子式与离子符号相同.
B.阳离子的电子式与离子符号相同;
C.阳离子的电子式与离子符号相同;
D.阳离子的电子式与离子符号相同.
解答:
解:A.氯原子最外层7个电子,氯离子最外层8个电子,故A错误;
B.镁离子的电子式为Mg2+,故B错误;
C.氢离子的电子式为H+,故C错误;
D.钠离子的电子式为Na+,故D正确.
故选D.
B.镁离子的电子式为Mg2+,故B错误;
C.氢离子的电子式为H+,故C错误;
D.钠离子的电子式为Na+,故D正确.
故选D.
点评:本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 | ||||
B、NH4HCO3(s)
| ||||
| C、因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可单独作为反应自发性的判据 | ||||
| D、在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
将8gNaOH固体溶解在水里,配得1L溶液,从中取出10mL,这10mL溶液的物质的量浓度是( )
| A、2mol/L |
| B、0.2 mol/L |
| C、0.02 mol/L |
| D、20 mol/L |
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | ||||
B、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | ||||
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
下列有关化学基本概念的判断依据,正确的是( )
| A、溶液与胶体:本质区别是否均一、透明 |
| B、纯净物与混合物:是否仅含有一种物质 |
| C、氧化还原反应与非氧化还原反应:是否有单质参加 |
| D、强电解质与弱电解质:化合物溶液导电能力是否强 |
某物质A加热时按下式分解:2A═4B↑+2C↑+D↑,现测得由生成物组成的混合气体对H2的相对密度为11.43.则反应物A的相对分子质量为( )
| A、22.86 |
| B、11.43 |
| C、80.01 |
| D、160.2 |
物质的性质决定用途,下列过程不是利用物质化学性质的是( )
| A、用新制Cu(OH)2检验尿糖 |
| B、用糯米、酒曲和水制甜酒 |
| C、用食醋除去水壶中的水垢 |
| D、苯使溴水褪色 |
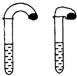 (1)高中教材中有这样一个实验:如图,在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下:
(1)高中教材中有这样一个实验:如图,在两支试管中分别加入3mL稀盐酸,将两个各装有0.3g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口.将气球内的NaHCO3或Na2CO3粉末同时倒入试管中,观察到现象如下: