题目内容
12.标况下,物质的量比为2:1的SO2和CO2的混合气体,其平均摩尔质量为57.3g/mol.分析 根据平均摩尔质量M=$\frac{m}{n}$结合m=nM来计算即可.
解答 解:平均摩尔质量M=$\frac{m}{n}$=$\frac{2mol×64g/mol+1mol×44g/mol}{2mol+1mol}$g/mol=57.3g/mol.
故答案为:57.3g/mol.
点评 本题考查学生有关物质的量、质量的计算等知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
3. 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、K+、Na+、Fe3+、Mg2+、Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀的物质的量与加入盐酸体积的关系如图所示.已知:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,下列结论不正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、K+、Na+、Fe3+、Mg2+、Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀的物质的量与加入盐酸体积的关系如图所示.已知:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,下列结论不正确的是( )
 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、K+、Na+、Fe3+、Mg2+、Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀的物质的量与加入盐酸体积的关系如图所示.已知:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,下列结论不正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、K+、Na+、Fe3+、Mg2+、Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀的物质的量与加入盐酸体积的关系如图所示.已知:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,下列结论不正确的是( )| A. | 原混合溶液中一定含有的离子是OH-、CO32-、AlO2-、SiO32-、Al3+ | |
| B. | AB段反应的离子方程式是H++CO32-═HCO3-,H++HCO3-═CO2↑+H2O | |
| C. | AB段之前反应的离子方程式是AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | |
| D. | K+、Na+两种离子肯定存在其中一种 |
20.关于符号ZAX2+的判断不正确的是( )
| A. | 它可以表示一个阳离子 | B. | X表示元素的符号 | ||
| C. | Z表示质子数,A则表示质量数 | D. | 此微粒含有电子总数为Z+2 |
4.下列关于化学用语的表示正确的是( )
| A. | 氢氧化钠的电子式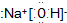 | |
| B. | 质子数为29、中子数为35的铜原子${:}_{29}^{35}$Cu | |
| C. | 氯离子的结构示意图: | |
| D. | 对苯二酚的结构简式: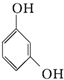 |
1.实验测得某溶液中仅含有K+、Cu2+、SO42-、Cl-四种离子.,其中K+、Cu2+、Cl-三种离子的个数比为4:5:8,则K+与SO42-的物质的量比为( )
| A. | 4:3 | B. | 4:1 | C. | 2:3 | D. | 2:1 |
2.下列关于氢氧化铁胶体的叙述中,错误的是( )
| A. | 向沸水中滴加饱和氯化铁溶液可制取氢氧化铁胶体 | |
| B. | 可见光透过氢氧化铁胶体时,发生丁达尔现象 | |
| C. | 氢氧化铁胶体放置一段时间后会产生沉淀 | |
| D. | 氢氧化铁胶粒的大小在1-100nm之间 |


 .
. .
. .
.