题目内容
将2mol SO2和1mol O2气体在1L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2(g)?2SO3 (g).若经过2s后测得SO3的浓度为0.6mol/L.试计算:
(1)求SO3的化学反应速率V(SO3)为多少?
(2)求2s时的O2浓度?
(1)求SO3的化学反应速率V(SO3)为多少?
(2)求2s时的O2浓度?
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:利用三段式计算各组成的浓度变化量、2s时各组成的浓度,若经过2s后测得SO3的浓度为0.6mol/L,物质的量=0.6mol/L×1L=0.6mol;
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
根据v=
计算v(SO3),根据c=
计算浓度.
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
根据v=
| △c |
| △t |
| n |
| V |
解答:
解:利用三段式计算各组成的浓度变化量、2s时各组成的浓度,若经过2s后测得SO3的浓度为0.6mol/L,物质的量=0.6mol/L×1L=0.6mol;
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
(1)SO3的化学反应速率V(SO3)=
=0.3mol/(L.s),
答:SO3的化学反应速率V(SO3)为0.3mol/(L.s);
(2)2s时的O2浓度=
=0.7mol/L;
答:2s时的O2浓度0.7mol/L.
2SO2(g)+O2(g)?2SO3 (g)
起始量(mol) 2 1 0
变化量(mol) 0.6 0.3 0.6
2s量(mol) 1.4 0.7 0.6
(1)SO3的化学反应速率V(SO3)=
| ||
| 2s |
答:SO3的化学反应速率V(SO3)为0.3mol/(L.s);
(2)2s时的O2浓度=
| 0.7mol |
| 1L |
答:2s时的O2浓度0.7mol/L.
点评:本题考查了化学反应三段式计算应用,主要是反应速率和浓度概念的计算,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
根据下表信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径 | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A、氢化物的稳定性为H2T<H2R |
| B、氢氧化物碱性:L(OH)2<Q(OH)2 |
| C、L2+与R2-的核外电子数相等 |
| D、M与T形成的化合物具有两性 |
 (1)用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出丁烷燃烧的热化学方程式
(1)用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出丁烷燃烧的热化学方程式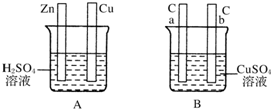 对如图中电极加以必要的连接并填空:
对如图中电极加以必要的连接并填空: